题目内容
前18号元素中最外层电子数是次外层电子数一半的元素有( )
| A、1种 | B、2种 | C、3种 | D、4种 |
考点:原子核外电子排布
专题:
分析:1~18 号元素,处于短周期,即一、二、三周期,讨论元素所处周期,根据最外层电子数是次外层电子数一半确定符合条件的元素.
解答:
解:1~18 号元素,处于短周期,即一、二、三周期,最外层电子数是次外层电子数一半,至少有2个电子层:
若处于第二周期,则次外层电子数为2,最外层电子数为1,为Li元素;
若处于第三周期,则次外层电子数为8,最外层电子数为4,为Si元素,
故符合条件的元素共有2种,
故选B.
若处于第二周期,则次外层电子数为2,最外层电子数为1,为Li元素;
若处于第三周期,则次外层电子数为8,最外层电子数为4,为Si元素,
故符合条件的元素共有2种,
故选B.
点评:本题考查结构位置关系应用,比较基础,注意核外电子排布规律的理解掌握.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
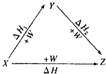 X、Y、Z、W有如图所示的转化关系,已知焓变:△H=△H1+△H2,则X、Y可能是( )
X、Y、Z、W有如图所示的转化关系,已知焓变:△H=△H1+△H2,则X、Y可能是( )①C、CO ②Na2CO3、NaHCO3 ③AlCl3、Al(OH)3 ④FeBr2、FeBr3.
| A、①②③④ | B、①③ |
| C、②④ | D、①②③ |
已知I-、Fe2+、SO2和H2O2均有还原性,它们在酸性溶液中还原性的强弱顺序为Fe2+<H2O2<I-<SO2,则下列反应不能发生的是( )
| A、2Fe3++SO2+2H2O═2Fe2++SO42-+4H+ |
| B、H2O2+H2SO4═SO2+O2+2H2O |
| C、I2+SO2+2H2O═H2SO4+2HI |
| D、2Fe3++H2O2═2Fe2++O2↑+2H+ |
下列各组中粒子在指定溶液中能大量共存的是( )
| A、0.lmol.L-1氯化铁溶液中Ca2+、Ba2+、Na+、HCO3- | ||
| B、氯水中 H2SO3、K+、SO42-、NH4+ | ||
| C、与镁反应只产生氢气的溶液中 NO3-、C1-、H+、A13+ | ||
D、
|
铅蓄电池是广泛应用于汽车、柴油机车等的启动电源.下列有关铅蓄电池的说法不正确的是( )
| A、铅蓄电池在充电时,原来负极发生的反应是:Pb+SO42--2e-?PbSO4 |
| B、铅蓄电池的电解质溶液是硫酸溶液,在放电过程中,它的浓度逐渐降低 |
| C、铅蓄电池在放电时,电子从Pb通过导线流向PbO2 |
| D、铅蓄电池放电时为原电池,充电时为电解池 |
在强酸性无色透明溶液中,下列各组离子不能大量共存的是( )
| A、Fe3+、K+、Cl-、MnO4- |
| B、K+、Na+、NO3-、Cl- |
| C、Zn2+、Al3+、SO42-、Cl- |
| D、Ba2+、NH4+、Cl-、NO3- |
下列各组物质中分子数相同的是( )
| A、2 L CO和2 L CO2 |
| B、9 g H2O和标准状况下11.2 L CO2 |
| C、标准状况下1 mol O2和22.4 L H2O |
| D、0.2 mol H2和4.48 L HCl气体 |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、在常温、常压下,11.2 L N2含有的分子数为0.5 NA |
| B、标准状况下,22.4 L H2和O2的混合物所含分子数为NA |
| C、标准状况下,18 g H2O的体积是22.4 L |
| D、1 mol SO2的体积是22.4 L |
下列有关物质的分类正确的是( )
| A、混合物:空气、矿泉水、水银、碘酒 |
| B、碱:Ba(OH)2、NH3?H2O、烧碱、纯碱 |
| C、盐:醋酸钠、氯化铵、硫酸钡、FeSO4 |
| D、氧化物:H2O、CO、Fe3O4、HCOOH |