题目内容
某工厂用FeCl3溶液腐蚀镀有铜的绝缘板生产印刷电路.其化学原理为:2FeCl3+Cu→2FeCl2+CuCl2.某实验小组的同学对该厂生产印刷电路后所得的废液进行了分析:取50.00mL 废液,向其中加入足量的AgNO3溶液,析出沉淀43.05g.(假设反应前后溶液的体积变化均忽略不计)请回答:
(1)该厂使用的FeCl3溶液(原来的)物质的量浓度 .
(2)若向250.00mL废液中加入足量的铜粉,充分反应后,铜粉质量减轻9.6g.
①充分反应后的溶液中Cu2+的物质的量为 .
②原废液中各金属阳离子的物质的量浓度之比为 .
(要求:写出的金属阳离子与其物质的量浓度数值一一对应)
(1)该厂使用的FeCl3溶液(原来的)物质的量浓度
(2)若向250.00mL废液中加入足量的铜粉,充分反应后,铜粉质量减轻9.6g.
①充分反应后的溶液中Cu2+的物质的量为
②原废液中各金属阳离子的物质的量浓度之比为
(要求:写出的金属阳离子与其物质的量浓度数值一一对应)
考点:化学方程式的有关计算
专题:计算题
分析:(1)废液加入足量的AgNO3溶液,生成沉淀43.05g为AgCl质量,根据氯元素守恒计算溶液中n(FeCl3),根据c=
计算原废液中c(FeCl3);
(2)①若向250.00mL废液中加入足量的铜粉,充分反应后,铁离子完全反应,根据该厂使用的FeCl3溶液浓度和体积可计算铁离子的物质的量,再根据得失电子守恒计算、原子守恒计算反应后溶液中铜离子的物质的量;
②计算9.6g铜的物质的量为0.15mol,则250ml废液中含有Cu2+为0.25mol-0.15mol=0.1mol,由2Fe3++Cu=2Fe2++Cu2+计算生成0.1molCu2+时,反应后剩余的n(Fe3+)以及生成的n(Fe2+).
| n |
| V |
(2)①若向250.00mL废液中加入足量的铜粉,充分反应后,铁离子完全反应,根据该厂使用的FeCl3溶液浓度和体积可计算铁离子的物质的量,再根据得失电子守恒计算、原子守恒计算反应后溶液中铜离子的物质的量;
②计算9.6g铜的物质的量为0.15mol,则250ml废液中含有Cu2+为0.25mol-0.15mol=0.1mol,由2Fe3++Cu=2Fe2++Cu2+计算生成0.1molCu2+时,反应后剩余的n(Fe3+)以及生成的n(Fe2+).
解答:
解:(1)废液加入足量的AgNO3溶液,生成沉淀43.05g为AgCl质量,其物质的量=
=0.3mol,根据氯元素守恒,原溶液中n(FeCl3)=
n(AgCl)=
×0.3mol=0.1mol,故原废液中c(FeCl3)=
=2mol/L,
故答案为:2mol/L.
(2)①250ml该厂使用的FeCl3溶液中n(Fe3+)=n(FeCl3)=2 mol/L×0.25 L=0.5mol,与铜反应得到电子为0.5mol,同时有0.25mol铜失去0.5mol电子变为铜离子,
故答案为:0.25mol;
②9.6g铜的物质的量为
=0.15mol,则250ml废液中含有Cu2+为0.25mol-0.15mol=0.1mol.由2Fe3++Cu=2Fe2++Cu2+可知,
0.5molFe3+反应生成0.1molCu2+时消耗Fe3+0.2mol、生成0.2molFe2+,则废液中c(Fe3+):c(Fe2+):c(Cu2+)=n(Fe3+):n(Fe2+):n(Cu2+)=0.3mol:0.2mol:0.1mol=3:2:1,
故答案为:c(Fe3+):c(Fe2+):c(Cu2+)=3:2:1.
| 43.05g |
| 143.5g/mol |
| 1 |
| 3 |
| 1 |
| 3 |
| 0.1mol |
| 0.05L |
故答案为:2mol/L.
(2)①250ml该厂使用的FeCl3溶液中n(Fe3+)=n(FeCl3)=2 mol/L×0.25 L=0.5mol,与铜反应得到电子为0.5mol,同时有0.25mol铜失去0.5mol电子变为铜离子,
故答案为:0.25mol;
②9.6g铜的物质的量为
| 9.6g |
| 64g/mol |
0.5molFe3+反应生成0.1molCu2+时消耗Fe3+0.2mol、生成0.2molFe2+,则废液中c(Fe3+):c(Fe2+):c(Cu2+)=n(Fe3+):n(Fe2+):n(Cu2+)=0.3mol:0.2mol:0.1mol=3:2:1,
故答案为:c(Fe3+):c(Fe2+):c(Cu2+)=3:2:1.
点评:本题考查了溶液中离子浓度的大小计算,题目难度一般,注意运用得失电子守恒、原子守恒或离子反应方程式进行计算.

练习册系列答案
相关题目
某含铬(Cr2O72-)废水用硫酸亚铁铵[FeSO4?(NH4)2SO4?6H2O]处理,反应中铁元素和铬元素完全转化为沉淀.该沉淀经干燥后得到n mol FeO?FeyCrxO3.不考虑处理过程中的实际损耗,下列叙述错误的是( )
| A、消耗硫酸亚铁铵的物质的量为n(y+1)mol |
| B、处理废水中Cr2O72-的物质的量为nx mol或ny/3 mol |
| C、反应中发生转移的电子数为ny mol |
| D、在FeO?FeyCrxO3中,若x=0.5,则y=1.5 |
下列说法正确的是( )
| A、白磷分子呈正四面体,键角109°28′,1mol白磷含共价键6mol |
| B、石墨晶体呈层状结构,每个碳原子只有3个价电子形成共价键 |
| C、等质量的NO2 和N2O4所含的原子数不相同 |
| D、S8是分子晶体,8个硫原子在同一个平面上,摩尔质量为256g |
有一种混合气体,它可能由CO、CO2、SO2、HCl中的一种或多种气体组成.该气体依次通过下列物质的现象如下:缓慢通过澄清石灰水无白色沉淀出现;通过品红溶液,溶液红色褪去;通过炽热的CuO,固体变为红色;通过澄清石灰水,出现白色沉淀.该混合气体组成的各说法中,正确的是( )
| A、肯定不含有CO2 |
| B、只含有SO2和CO |
| C、含有SO2、CO和CO2,可能含HCl |
| D、含HCl、SO2和CO,可能含CO2 |
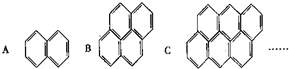 在沥青蒸气里含有多种稠环芳香烃,如图所示A、B、C …,
在沥青蒸气里含有多种稠环芳香烃,如图所示A、B、C …,