题目内容
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A、18g D2O中含有的氧原子数为NA |
| B、实验室用2mol的浓HCl在加热条件下与足量的MnO2反应,转移的电子数为NA |
| C、22.4L氯化氢溶于水可电离出1mol Cl- |
| D、由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为2NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.重水的摩尔质量为20g/mol,18g重水的物质的量为0.9mol,含有0.9mol氧原子;
B.消耗2mol氯化氢能够生成0.5mol氯气,转移了1mol电子;稀盐酸不与二氧化锰反应,生成氯气的物质的量小于0.5mol;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氯化氢的物质的量;
D.二氧化碳和氧气分子中都含有2个氧原子,NA个二者的混合气体则含有2NA个氧原子.
B.消耗2mol氯化氢能够生成0.5mol氯气,转移了1mol电子;稀盐酸不与二氧化锰反应,生成氯气的物质的量小于0.5mol;
C.没有告诉在标况下,不能使用标况下的气体摩尔体积计算氯化氢的物质的量;
D.二氧化碳和氧气分子中都含有2个氧原子,NA个二者的混合气体则含有2NA个氧原子.
解答:
解:A.18g重水的物质的量为0.9mol,0.9mol重水中含有0.9mol氧原子,含有的氧原子数为0.9NA,故A错误;
B.2mol浓盐酸完全反应最多生成0.5mol氯气,由于随着反应的进行,浓盐酸变成稀盐酸,反应停止,所以反应生成的氯气小于0.5mol,转移的电子小于1mol,转移的电子数小于NA,故B错误;
C.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氯化氢的物质的量,故C错误;
D.CO2和O2组成的混合物中共有NA个分子,由于二氧化碳和氧气中都含有2个氧原子,则混合气体中含有的氧原子数为2NA,故D正确;
故选D.
B.2mol浓盐酸完全反应最多生成0.5mol氯气,由于随着反应的进行,浓盐酸变成稀盐酸,反应停止,所以反应生成的氯气小于0.5mol,转移的电子小于1mol,转移的电子数小于NA,故B错误;
C.不是标准状况下,不能使用标况下的气体摩尔体积计算22.4L氯化氢的物质的量,故C错误;
D.CO2和O2组成的混合物中共有NA个分子,由于二氧化碳和氧气中都含有2个氧原子,则混合气体中含有的氧原子数为2NA,故D正确;
故选D.
点评:本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,选项B为易错点,注意稀盐酸不与二氧化锰反应.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
一定量的某有机物完全燃烧后,将燃烧产物通过足量的石灰水,经过滤可得沉淀10g,有机物燃烧产生2.7g水,则此有机物不可能是( )
| A、乙烷 | B、乙烯 | C、乙醇 | D、乙二醇 |
下列物质中含有共价键的离子化合物是( )
| A、Ba(OH)2 |
| B、CaCl2 |
| C、H2O |
| D、H2 |
在一定温度下的定容密闭容器中,A(固)+2B(气)?C(气)+D(气)当下列物理量不再变化时,不能表明反应已达平衡的是( )
| A、C的物质的量浓度 |
| B、混合气体的压强 |
| C、混合气体的密度 |
| D、混合气体的平均分子量 |
有关键能数据如下表所示:
则晶体硅在氧气中燃烧的热化学方程式为Si(s)+O2(g)═SiO2(s);△H=-989.2kJ?mol-1,则x的值为
( )
| 化学键 | Si-O | O=O | Si=Si |
| 键能kJ?mol-1 | x | 498.8 | 176 |
( )
| A、460 | B、920 |
| C、1165.2 | D、423.3 |
等物质的量的氢气和氦气具有相同的( )
| A、质量 | B、原子数 |
| C、质子数 | D、体积 |
 北京2008年奥运会的理念是“绿色奥运”“人文奥运”.举办“人文奥运”的一个重要体现是,禁止运动员服用兴奋剂.有一种兴奋剂的结构简式为,有关该物质的说法正确的是( )
北京2008年奥运会的理念是“绿色奥运”“人文奥运”.举办“人文奥运”的一个重要体现是,禁止运动员服用兴奋剂.有一种兴奋剂的结构简式为,有关该物质的说法正确的是( )| A、遇FeCl3溶液显紫色,因为该物质与苯酚属于同系物 |
| B、滴入KMnO4酸性溶液,观察到紫色褪去,可证明分子中存在双键 |
| C、1mol该物质与足量的碳酸氢钠反应,产生3mol CO2 |
| D、1mol该物质与浓溴水和H2反应时,最多消耗Br2和H2的物质的量分别为4 mol、7 mol |
下列有关实验操作的叙述正确的是( )
| A、将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中 |
| B、某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| C、NaCl溶液蒸发结晶时,蒸发皿中刚好有晶体析出时即停止加热 |
| D、向AlCl3溶液中滴加氨水,会产生白色沉淀,再加入NaHSO4溶液,沉淀不消失 |
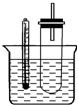 溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物.某同学依据溴乙烷的性质,用如图实验装置(铁架台、酒精灯略)验证取代反应和消去反应的产物,请你一起参与探究.