题目内容
7.下列有关说法正确的是( )| A. | 铜的金属活动性比铁弱,可以用铜罐代替铁罐盛装和运输浓硝酸 | |
| B. | 明矾净水与铁粉作食品的脱氧剂都利用了物质的还原性 | |
| C. | 钢瓶可以运输液氯 | |
| D. | 用氧化铝制成的耐高温坩埚可以用于熔融氢氧化钠 |
分析 A.依据铜能够与浓硝酸反应,浓硝酸遇到铁发生钝化解答;
B.依据明矾净水的原理解答;
C.干燥的氯气与铁不反应;
D.氧化铝为两性氧化物,能够与氢氧化钠反应.
解答 解:A.浓硝酸具有强氧化性,遇到铁发生钝化,可以用铁罐盛放运输浓硝酸,铜能够与浓硝酸反应,不能用铜罐代替铁罐盛装和运输浓硝酸,故A错误;
B.明矾净水是因为明矾电离产生的铝离子水解生成的氢氧化铝具有吸附性,故B错误;
C.干燥的氯气与铁不反应,可以运输液氯,故C正确;
D.氧化铝为两性氧化物,能够与氢氧化钠反应,所以不能够用氧化铝坩埚熔融氢氧化钠,故D错误;
故选:C.
点评 本题考查了元素化合物知识,明确浓硝酸、盐类水解的性质、两性氧化物的性质是解题关键,题目难度不大,注意钝化属于化学变化.

练习册系列答案
相关题目
17.${\;}_{6}^{13}$C和${\;}_{6}^{14}$C是碳元素的两种核素,它们具有不同的( )
| A. | 质子数 | B. | 中子数 | C. | 电子数 | D. | 核外电子排布 |
18.下列操作不能用于检验NH3的是( )
| A. | 气体使酚酞试液变红 | B. | 气体能使湿润的红色石蕊试纸变蓝 | ||
| C. | 气体与蘸有浓H2SO4的玻璃棒靠近 | D. | 气体与蘸有浓盐酸的玻璃棒靠近 |
15.分子式为C3H4Cl2且含有 结构的有机物的同分异构体共有(不考虑立体异构)( )
结构的有机物的同分异构体共有(不考虑立体异构)( )
 结构的有机物的同分异构体共有(不考虑立体异构)( )
结构的有机物的同分异构体共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
2.为了除去硝酸钾晶体中所含的硫酸钙和硫酸镁,先将它配成溶液,然后加入KOH、K2CO3、Ba(NO3)2等试剂,配以过滤、蒸发结晶等操作,制成纯净的硝酸钾晶体,其加入试剂的顺序正确的是( )
| A. | Ba(NO3)2--KOH--K2CO3--HNO3 | B. | Ba(NO3)2--KOH--HNO3--K2CO3 | ||
| C. | KOH--K2CO3--Ba(NO3)2--HNO3 | D. | K2CO3--Ba(NO3)2--KOH--HNO3 |
12.25℃时,在①0.01mol/L的盐酸,②pH=2的醋酸,③pH=12的氨水,④0.01mol/L的NaOH溶液4种溶液中,由水电离出的c(H+)的大小关系是( )
| A. | ②>①>④>③ | B. | ①=②=③=④ | C. | ②=③>①=④ | D. | ②<①<③<④ |
19.S2C12是橡胶工业上常用的硫化剂,是一种金黄色液体.
已知:①S2C12不稳定,进一步氯化可得SCl2;②S2Cl2、SCl2都能与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+6HCl;③几种物质的熔沸点如表:
如图是实验室中通过向熔融的单质硫中通入少量氯气制取S2Cl2的装置(部分夹持、加热装置已略去).
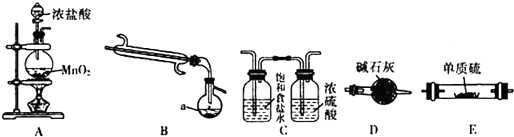
(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验证明所得产品中是否含有杂质SCl2取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.
已知:①S2C12不稳定,进一步氯化可得SCl2;②S2Cl2、SCl2都能与水反应,2S2Cl2+2H2O═3S↓+SO2↑+4HCl,3SCl2+4H2O═2S↓+H2SO4+6HCl;③几种物质的熔沸点如表:
| 物质 | S | SCl2 | S2Cl2 |
| 熔点/℃ | 445 | 59 | 137 |
| 沸点/℃ | 113 | -122 | -77 |

(1)B装置中仪器a的名称蒸馏烧瓶.
(2)装置的连接顺序是(每个装置只能使用一次)ACEBD.
(3)装置D的作用是防止空气中的水蒸气进入装置B,吸收多余的氯气.
(4)实验中先点燃A装置酒精灯制取Cl2,当当E中充满黄绿色的气体时,说明排净空气,再点燃E处酒精灯.
(5)由实验粗产品获得纯净的S2Cl2,需要进行的操作是蒸馏,该操作的温度范围是59℃~137℃.
(6)请设计实验证明所得产品中是否含有杂质SCl2取少量产品加入试管中,再加入适量蒸馏水,振荡、静置.取少量上层清夜,滴加氯化钡溶液,若有白色沉淀生成,证明有S2Cl2,否则无S2Cl2.
16.下列物质提纯的方法中,正确的是( )
| A. | 氯化铵溶液中含有少量的氯化铁,加入氢氧化钠溶液,过滤 | |
| B. | 用NaOH溶液除去CO中的少量CO2 | |
| C. | 将H2和O2混合气体通过炽热的CuO以除去氧气中的氢气 | |
| D. | H2S气体中含有水蒸气,将混合气体通过含有浓硫酸的洗气瓶 |
15.0.3mol Cu2S与足量的浓HNO3反应,生成Cu(NO3)2、H2SO4、NO、H2O,则参加反应的硝酸中,未被还原的硝酸的量是( )
| A. | 75.3g | B. | 2.2mol | C. | 1.2mol | D. | 1mol |