题目内容
已知Ga和As元素分别位于元素周期表的第13和15纵行.砷化镓是一种半导体材料,请回答下列问题:
(1)根据周期表中Ga、As所在的位置,写出砷化镓的化学式: ,其中镓元素的化合价为 .
(2)写出Ga原子处于基态时的核外电子排布式: .
(3)AsH3是As的氢化物,该分子的空间构型为 ,中心原子As的杂化方式为 .
(1)根据周期表中Ga、As所在的位置,写出砷化镓的化学式:
(2)写出Ga原子处于基态时的核外电子排布式:
(3)AsH3是As的氢化物,该分子的空间构型为
考点:元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)Ga和As元素分别位于元素周期表的第13和15纵行,Ga位于第IIIA族、As位于第VA族,As的电负性大于Ga,所以二者相互化合物时,As为-3价、Ga为+3价;
(2)Ga为31号元素,其原子核外有31个电子,根据构造原理书写其基态核外电子排布式;
(3)根据价层电子对互斥理论确定砷化氢分子空间构型、中心原子杂化方式.
(2)Ga为31号元素,其原子核外有31个电子,根据构造原理书写其基态核外电子排布式;
(3)根据价层电子对互斥理论确定砷化氢分子空间构型、中心原子杂化方式.
解答:
解:(1)Ga和As元素分别位于元素周期表的第13和15纵行,Ga位于第IIIA族、As位于第VA族,As的电负性大于Ga,所以二者相互化合物时,As为-3价、Ga为+3价,所以砷化镓的化学式为GaAs,故答案为:GaAs;+3;
(2)Ga为31号元素,其原子核外有31个电子,根据构造原理知其基态核外电子排布式为1s22s22p63s23p63d104s24p1,故答案为:1s22s22p63s23p63d104s24p1;
(3)AsH3分子中价层电子对个数=3+
×(5-3×1)=4且含有一个孤电子对,所以其空间构型为三角锥形,As原子采用sp3杂化,故答案为:三角锥形;sp3.
(2)Ga为31号元素,其原子核外有31个电子,根据构造原理知其基态核外电子排布式为1s22s22p63s23p63d104s24p1,故答案为:1s22s22p63s23p63d104s24p1;
(3)AsH3分子中价层电子对个数=3+
| 1 |
| 2 |
点评:本题考查了原子结构及元素性质,涉及原子杂化方式的判断、微粒空间构型的判断、核外电子排布式书写等知识点,根据价层电子对互斥理论、构造原理等知识点来分析解答,题目难度不大.

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目
X、Y、Z三种元素在周期表中,X、Y同主族,Y和Z同周期,它们的原子的最外层电子数之和为16,则这三种元素可能是( )
| A、Na、K、Ca |
| B、N、P、S |
| C、F、Cl、S |
| D、O、S、Cl |
在容积不变的密闭容器中,在一定条件下发生反应2A?B(g)+C(s),且达到化学平衡.当升高温度时容器内气体的密度增大.则下列判断正确的是( )
| A、若正反应是吸热反应,则A为非气态 |
| B、若正反应是放热反应,则A为气态 |
| C、若在平衡体系中加入少量C,该平衡向逆反应方向移动 |
| D、压强对该平衡的移动无影响 |

 、
、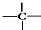 中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示.例如:
中的碳原子分别称为伯、仲、叔、季碳原子,数目分别用n1、n2、n3、n4表示.例如: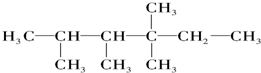 分子中,n1=6、n2=1、n3=2、n4=1.试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)中各原子数的关系.
分子中,n1=6、n2=1、n3=2、n4=1.试根据不同烷烃的组成结构,分析出烷烃(除甲烷外)中各原子数的关系.