题目内容
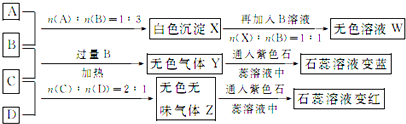
现有四瓶丢失标签的NaOH、Na2CO3、AlCl3、NH4HSO4溶液,为鉴别四瓶溶液,将四瓶溶液编号为A、B、C、D进行实验.实验过程和记录如图所示(无关物质已经略去):
(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为 、 .
(2)D溶液pH 7(填“大于”、“小于”或“等于”),原因是(用离子方程式表示) .
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是 .(用化学式表示)
(4)等物质的量浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者 后者(填“<”、“>”或“=”).
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是 .

(1)A、W的溶液分别加热蒸干并灼烧最后所得固体为
(2)D溶液pH
(3)等物质的量浓度的A、B、C、D溶液pH由大到小的顺序是
(4)等物质的量浓度的C溶液与NH4Cl溶液相比较,c(NH4+):前者
(5)若B、C的稀溶液混合后(不加热)溶液呈中性,则该溶液中离子浓度从大到小的顺序是
考点:几组未知物的检验
专题:物质检验鉴别题
分析:由A、B反应流程图及比例关系可推A为AlCl3,B为NaOH,由B、C反应流程图知,Y为NH3,C应该为铵盐,所以C为NH4HSO4,D就为Na2CO3气体,Z为CO2,
(1)加热促进盐类的水解,根据盐类水解原理分析;
(2)含有弱离子的盐可以水解,根据水解原理确定溶液的酸碱性;
(3)根据酸、碱的电离以及盐类的水解的角度比较溶液pH的大小;
(4)从盐类水解的影响因素以及平衡移动的角度分析;
(5)从溶液电荷守恒的角度进行回答判断.
(1)加热促进盐类的水解,根据盐类水解原理分析;
(2)含有弱离子的盐可以水解,根据水解原理确定溶液的酸碱性;
(3)根据酸、碱的电离以及盐类的水解的角度比较溶液pH的大小;
(4)从盐类水解的影响因素以及平衡移动的角度分析;
(5)从溶液电荷守恒的角度进行回答判断.
解答:
解:由A、B反应流程图及比例关系可推A为AlCl3,B为NaOH,由B、C反应流程图知,Y为NH3,C应该为铵盐,所以C为NH4HSO4,D就为Na2CO3气体Z为CO2,故答案为:AlCl3;NaOH;NH4HSO4;Na2CO3;
(1)A是AlCl3,AlCl3水解:Al3++3H2O?Al(OH)3+3H+,灼烧:2Al(OH)3
Al2O3+3H2O;AlCl3水解产物受热分解得到的是Al2O3和HCl,最后HCl完全逸到空气中;W是NaAlO2,水解AlO2-+H2O?Al(OH)3+OH-,由于OH-的存在,Al(OH)3不能沉淀下来,最后得到NaAlO2;故答案为:Al2O3;NaAlO2;
(2)D是Na2CO3,由于CO32-水解:CO32-+H2O?HCO3-+OH-而呈碱性,故pH>7,故答案为:大于;CO32-+H2O?HCO3-+OH-;
(3)A、B、C、D四种溶液,其中NaOH和Na2CO3呈碱性的pH>7,而且NaOH碱性>Na2CO3,AlCl3和NH4HSO4呈酸性,pH<7,NH4HSO4酸性>AlCl3,所以等物质的量浓度A、B、C、D的pH由大到小的顺序是NaOH>Na2CO3>AlCl3>NH4HSO4,故答案为:NaOH>Na2CO3>AlCl3>NH4HSO4;
(4)等物质的量浓度的NH4HSO4与NH4Cl溶液,NH4HSO4电离出的H+对NH4+的水解起到抑制作用,所以c(NH4+):前者>后者,故答案为:>;
(5)B、C的稀溶液混合后(不加热)溶液呈中性,则溶液中存在硫酸钠、硫酸铵以及氨水等溶质,混合溶液呈中性,则c(H+)=c(OH-),由电荷守恒有c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-).
(1)A是AlCl3,AlCl3水解:Al3++3H2O?Al(OH)3+3H+,灼烧:2Al(OH)3
| ||
(2)D是Na2CO3,由于CO32-水解:CO32-+H2O?HCO3-+OH-而呈碱性,故pH>7,故答案为:大于;CO32-+H2O?HCO3-+OH-;
(3)A、B、C、D四种溶液,其中NaOH和Na2CO3呈碱性的pH>7,而且NaOH碱性>Na2CO3,AlCl3和NH4HSO4呈酸性,pH<7,NH4HSO4酸性>AlCl3,所以等物质的量浓度A、B、C、D的pH由大到小的顺序是NaOH>Na2CO3>AlCl3>NH4HSO4,故答案为:NaOH>Na2CO3>AlCl3>NH4HSO4;
(4)等物质的量浓度的NH4HSO4与NH4Cl溶液,NH4HSO4电离出的H+对NH4+的水解起到抑制作用,所以c(NH4+):前者>后者,故答案为:>;
(5)B、C的稀溶液混合后(不加热)溶液呈中性,则溶液中存在硫酸钠、硫酸铵以及氨水等溶质,混合溶液呈中性,则c(H+)=c(OH-),由电荷守恒有c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-),故答案为:c(Na+)>c(SO42-)>c(NH4+)>c(H+)=c(OH-).
点评:本题考查物质的检验及鉴别,题目难度中等,本题侧重于盐类的水解考查,学习中注意把握相关知识.

练习册系列答案
相关题目
实验室中需要配制2mol/L的NaCl溶液950mL,配制时应选用的容量瓶的规格和称取的NaCl的质量分别是( )
| A、950 mL 111.2 g |
| B、500 mL 117.0g |
| C、1000 mL 117.0 g |
| D、1000 mL 111.2 g |
光导纤维被认为是20世纪最伟大的发明之一,它使信息高速公路在全球迅猛发展,它的发明者是被誉为“光纤之父”的华人科学家高锟.光导纤维的主要成分是( )
| A、CaCO3 |
| B、SiO2 |
| C、Na2SiO3 |
| D、CaSiO3 |

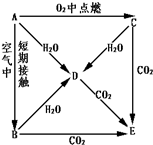 A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按如图所示关系相互转化,已知A金属为单质,C的焰色呈黄色.
A、B、C、D、E五种物质都含1~18号元素中的某一元素,它们按如图所示关系相互转化,已知A金属为单质,C的焰色呈黄色.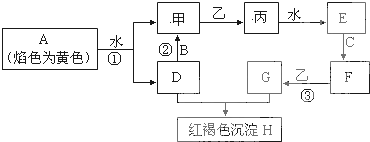
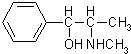 (1)药品分为处方药和非处方药.处方药是指必须在医生监控或指导下使用的药物,用符号
(1)药品分为处方药和非处方药.处方药是指必须在医生监控或指导下使用的药物,用符号