题目内容
 (1)铅蓄电池是典型的二次电池,由于铅蓄电池的性能优良、价格低廉、安全可靠,可多次充放电,所以在生产生活中使用广泛,总反应式是pb+pbo2+4H++2SO42-
(1)铅蓄电池是典型的二次电池,由于铅蓄电池的性能优良、价格低廉、安全可靠,可多次充放电,所以在生产生活中使用广泛,总反应式是pb+pbo2+4H++2SO42-| 放电 |
| 充电 |
| 电池 | 电解池 | |
| A | H+移向pb电极 | H+移向pb电极 |
| B | 每消耗3mol pb | 生成2molAl2O3 |
| C | 正极:pbO2+4H++2e-=pb2++2H2O | 阳极:2AL+3H2O-6e-═AL2O3+6H+ |
| D |  | 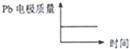 |
电解
电池:Pb(s)+PbO2(s)+2H2SO4(aq)═2PbSO4(s)+2H2O(l)
电解池:2Al+3H2O═Al2O3+3H2↑电解过程中,以下判断正确的是
(3)某种可充电聚合物锂离子电池放电时的反应为
Li1-xCoO2+LixC6=6C+LiCoO2,其工作原理示意图如图,下列说法不正确的是
考点:常见化学电源的种类及其工作原理,化学电源新型电池
专题:电化学专题
分析:(1)放电时为原电池,负极上铅失电子发生氧化会反应,正极上氧化铅得电子;充电时,阴极上硫酸铅得电子生成铅;
(2)A.原电池放电时,溶液中阳离子向正极移动;
B.串联电池中转移电子数相等;
C.原电池正极上生成硫酸铅;
D.原电池中铅电极上生成硫酸铅,电解池中阴极生成氢气;
(3)放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,Co元素的化合价升高,C元素的化合价降低,结合原电池中负极发生氧化反应,正极发生还原反应来解答.
(2)A.原电池放电时,溶液中阳离子向正极移动;
B.串联电池中转移电子数相等;
C.原电池正极上生成硫酸铅;
D.原电池中铅电极上生成硫酸铅,电解池中阴极生成氢气;
(3)放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,Co元素的化合价升高,C元素的化合价降低,结合原电池中负极发生氧化反应,正极发生还原反应来解答.
解答:
解:(1)放电时,该装置是原电池,负极上铅失电子发生氧化会反应,正极是二氧化铅得电子生成硫酸铅,电极反应式为PbO2+SO42-+2e-+4H+═PbSO4+2H2O,充电时,阴极上电极反应式为PbSO4+2e-=Pb+SO42-,
故答案为:Pb;PbO2+SO42-+2e-+4H+═PbSO4+2H2O;bSO4+2e-=Pb+SO42-;
(2)A.原电池中,溶液中氢离子向正极,即向二氧化铅电极移动,故A错误;
B.串联电池中转移电子数相等,每消耗3molPb,根据电子守恒生成lmolAl2O3,故B错误;
C.原电池正极上二氧化铅得电子生成硫酸铅,则正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,故C错误;
D.原电池中铅作负极,负极上铅失电子和硫酸根离子反应生成难溶性的硫酸铅,所以质量增加,在电解池中,Pb阴极,阴极上氢离子得电子生成氢气,所以铅电极质量不变,故D正确;
故答案为:D;
(3)放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,Co元素的化合价升高,C元素的化合价降低,
A.C元素的化合价升高,则放电时LixC6发生氧化反应,故A正确;
B.充电时,为电解装置,阳离子向阴极移动,则Li+通过阳离子交换膜从右向左移动,故B错误;
C.充电时负极与阴极相连,将电池的负极与外接电源的负极相连,故C正确;
D.正极上Co元素化合价降低,放电时,电池的正极反应为:Li1-xCoO2+xLi++xe-═LiCoO2,故D正确;
故答案为:B.
故答案为:Pb;PbO2+SO42-+2e-+4H+═PbSO4+2H2O;bSO4+2e-=Pb+SO42-;
(2)A.原电池中,溶液中氢离子向正极,即向二氧化铅电极移动,故A错误;
B.串联电池中转移电子数相等,每消耗3molPb,根据电子守恒生成lmolAl2O3,故B错误;
C.原电池正极上二氧化铅得电子生成硫酸铅,则正极:PbO2+4H++SO42-+2e-=PbSO4+2H2O,故C错误;
D.原电池中铅作负极,负极上铅失电子和硫酸根离子反应生成难溶性的硫酸铅,所以质量增加,在电解池中,Pb阴极,阴极上氢离子得电子生成氢气,所以铅电极质量不变,故D正确;
故答案为:D;
(3)放电时的反应为Li1-xCoO2+LixC6=6C+LiCoO2,Co元素的化合价升高,C元素的化合价降低,
A.C元素的化合价升高,则放电时LixC6发生氧化反应,故A正确;
B.充电时,为电解装置,阳离子向阴极移动,则Li+通过阳离子交换膜从右向左移动,故B错误;
C.充电时负极与阴极相连,将电池的负极与外接电源的负极相连,故C正确;
D.正极上Co元素化合价降低,放电时,电池的正极反应为:Li1-xCoO2+xLi++xe-═LiCoO2,故D正确;
故答案为:B.
点评:本题考查原电池原理和电解池原理 应用,明确电池反应中元素的化合价变化及电池的工作原理即可解答,注意与氧化还原反应的结合,题目难度中等.

练习册系列答案
 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案
相关题目
下列说法正确是( )
| A、1,3-戊二烯与溴发生加成反应的产物有3种 |
| B、乙烯和苯都能使溴水褪色,褪色的原因相同 |
| C、由于甲基对苯环的影响,使甲苯能使酸性高锰酸钾溶液褪色 |
| D、乙醇溶液呈中性,而苯酚溶液呈弱酸性,原因是苯环影响羟基,使羟基上的氢原子变得活泼了 |
下列指定反应的离子方程式正确的是( )
| A、用CH3COOH溶解CaCO3:CaCO3+2H+═Ca2++H2O+CO2↑ |
| B、Cu溶于稀硝酸HNO3:Cu+2H++NO3-═Cu2++NO2↑+H2O |
| C、(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-═Fe(OH)2↓ |
| D、向NaAlO2溶液中通入过量CO2:CO2+AlO2-+2H2O═Al(OH)3↓+HCO3- |
下列推断正确的是( )
| A、BF3是三角锥形分子 | ||
B、NH
 ,离子呈平面形结构 ,离子呈平面形结构 | ||
| C、CH4分子中的4个C-H键都是氢原子的1s轨道与碳原子的p轨道形成的s-p σ键 | ||
| D、CH4分子中的碳原子以4个sp3杂化轨道分别与4个氢原子的1s轨道重叠,形成4个s-sp3σ键 |

