题目内容
下列说法正确的是
①经分析某物质只含有一种元素,则该物质一定是单质;
②质子数相同,电子数也相同的粒子,不可能是一种分子和一种离子;
③碱性氧化物一定是金属氧化物;
④NO2不是酸性氧化物、Na2O2不属于碱性氧化物;
⑤两种盐反应一定生成两种新盐.
- A.①③④
- B.②③④
- C.②③⑤
- D.①③⑤
B
分析:①依据同素异形体是同元素组成的不同单质分析;
②因为质子数相同,电子数也相同的话不可能一种是分子,一种是离子,因为分子是电中性,而离子是带电的,所以说两者不可能同时一样的;
③碱性氧化物是和酸反应生成盐和水的氧化物.一定是金属氧化物;
④酸性氧化物是和减肥药生成盐和水的氧化物,碱性氧化物是和酸反应生成盐和水的氧化物,发生的都是复分解反应;
⑤氧化性盐和还原性盐会发生氧化还原反应、两种水解相互促进的盐反应生成气体沉淀等.
解答:①某物质只含有一种元素可以是同素异形体的混合物,故①错误;
②因为质子数相同,电子数也相同的话不可能一种是分子,一种是离子,因为分子是电中性,而离子是带电的,所以说两者不可能同时一样的,故②正确;
③依据碱性氧化物的概念和性质可知,碱性氧化物一定是金属氧化物,故③正确;
④依据酸性氧化物和碱性氧化物的概念分析判断,NO2不是酸性氧化物、Na2O2不属于碱性氧化物,故④正确;
⑤两种盐反应不一定生成两种新盐,如FeCl3和Na2S反应生成硫单质氯化亚铁和氯化钠;AlCl3+Na2S在水溶液中反应生成氢氧化铝沉淀和硫化氢气体,故⑤错误;
综上所述:②③④正确;
故选B.
点评:本题考查了酸碱盐氧化物概念的分析应用,主要考查同素异形体概念应用,物质性质的应用和反应特征.熟练掌握物质性质和化学概念的内涵是解题关键.
分析:①依据同素异形体是同元素组成的不同单质分析;
②因为质子数相同,电子数也相同的话不可能一种是分子,一种是离子,因为分子是电中性,而离子是带电的,所以说两者不可能同时一样的;
③碱性氧化物是和酸反应生成盐和水的氧化物.一定是金属氧化物;
④酸性氧化物是和减肥药生成盐和水的氧化物,碱性氧化物是和酸反应生成盐和水的氧化物,发生的都是复分解反应;
⑤氧化性盐和还原性盐会发生氧化还原反应、两种水解相互促进的盐反应生成气体沉淀等.
解答:①某物质只含有一种元素可以是同素异形体的混合物,故①错误;
②因为质子数相同,电子数也相同的话不可能一种是分子,一种是离子,因为分子是电中性,而离子是带电的,所以说两者不可能同时一样的,故②正确;
③依据碱性氧化物的概念和性质可知,碱性氧化物一定是金属氧化物,故③正确;
④依据酸性氧化物和碱性氧化物的概念分析判断,NO2不是酸性氧化物、Na2O2不属于碱性氧化物,故④正确;
⑤两种盐反应不一定生成两种新盐,如FeCl3和Na2S反应生成硫单质氯化亚铁和氯化钠;AlCl3+Na2S在水溶液中反应生成氢氧化铝沉淀和硫化氢气体,故⑤错误;
综上所述:②③④正确;
故选B.
点评:本题考查了酸碱盐氧化物概念的分析应用,主要考查同素异形体概念应用,物质性质的应用和反应特征.熟练掌握物质性质和化学概念的内涵是解题关键.

练习册系列答案
相关题目
设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A、1L 0.1mol?L-1 NaHSO3溶液中含有H+的数目为NA个 | B、常温常压下,等质量的CO2和N2O的气体体积相等 | C、60g组成为C2H4O2的有机物含C-H键数目为3NA个 | D、向HNO3溶液中加入过量的铁粉经充分反应后,转移的电子数目为3NA个 |
某氮肥厂氨氮废水中的氮元素多以NH4+ 和NH3?H2O的形式存在,经先期处理得到含HNO3的废水.一定条件下,向处理后的废水中加入CH3OH,将HNO3还原为N2.若该反应消耗32gCH3OH 转移6mol 电子,则下列说法正确的是( )
| A、硝酸分子中所有原子均达8电子结构 | B、参加反应的还原剂与氧化剂的物质的量之比为5:6 | C、常温下,向0.1mol/LNH3?H2O中加水稀释,则c(NH4+)/c(NH3?H2O) 将减小 | D、NH3分子与CO32-离子的空间构型相同 |
 关于铜锌原电池和电解CuCl2溶液的装置(如图),下列说法正确的是( )
关于铜锌原电池和电解CuCl2溶液的装置(如图),下列说法正确的是( )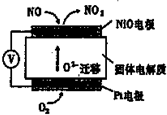 如图装置可用来监测空气中NO的含量,下列说法正确的是( )
如图装置可用来监测空气中NO的含量,下列说法正确的是( )