题目内容
20.将等体积、等物质的量浓度的 NaClO 与 NaOH 溶液混合,下列离子浓度关系正确的是( )| A. | c(ClO-)=c(OH-) | B. | c(ClO-)+c(OH-)═c(Na+) | ||
| C. | c(OH-)═c(HClO)+c(H+) | D. | 2c(ClO-)+2c(HClO)═c(Na+) |
分析 将等体积、等物质的量浓度的 NaClO 与 NaOH 溶液混合,根据电荷守恒,可知:c(ClO-)+c(OH-)═c(Na+)+c(H+),如果单一的 NaClO,根据组成可知:c(Na+)=c(ClO-)+c(HClO),而氢氧化钠与次氯酸钠提供等物质的量的钠离子,所以$\frac{1}{2}$c(Na+)=c(ClO-)+c(HClO),由此分析解答.
解答 解:A、次氯酸根离子水解产生氢氧根离子,则次氯酸根离子浓度减小,而氢氧根离子浓度增大,所以c(ClO-)<c(OH-),故A错误;
B、单一次氯酸钠中符合c(ClO-)+c(OH-)═c(Na+),而与等物质量的氢氧化钠混合,所以$\frac{1}{2}$c(Na+)=c(ClO-)+c(HClO),故B错误;
C、由B可知$\frac{1}{2}$c(Na+)=c(ClO-)+c(HClO),所以2c(ClO-)+2c(HClO)═c(Na+)…①,根据电荷守恒,可知:c(ClO-)+c(OH-)═c(Na+)+c(H+)…②,将①代入②可知:c(OH-)═c(ClO-)+2c(HClO)+c(H+),故C错误;
D、由B可知$\frac{1}{2}$c(Na+)=c(ClO-)+c(HClO),所以2c(ClO-)+2c(HClO)═c(Na+),故D正确;
故选D.
点评 本题综合离子浓度大小比较等相关知识,对于考生的要求较高,难度中等,侧重于考查学生对基础知识的综合应用能力,学生在解题中要注意守恒知识的应用.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案
相关题目
10.25℃时,将浓度均为0.1mol/L、体积分别为Va 和Vb 的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示. 下列说法正确的是( )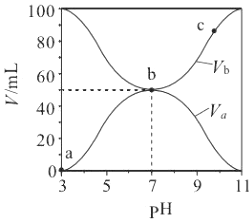

| A. | Ka(HA)的值与 Kb(BOH) 的值不相等 | |
| B. | b 点时,水电离出的 c(H+)=10-7mol/L | |
| C. | c 点时,c(A-)>c(B+) | |
| D. | a→c 过程中$\frac{c({A}^{-})}{c(O{H}^{-})•c(HA)}$不变 |
11.下列古诗诃描述的场景中发生的化学反应不属于氧化还原反应的是( )
| A.爆竹声中一岁除-黑火药受热爆炸 | B.烈火赞烧若等闲-石灰石分解 | C.蜡烛成灰泪始干-石蜡的燃烧 | D.炉火照天地,红星乱紫烟-铁的冶炼 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
8.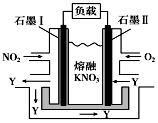 某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
 某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )
某燃料电池的工作原理如右图所示,该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,Y可循环使用.下列说法正确的是( )| A. | 该电池放电时K+向石墨Ⅰ电极迁移 | |
| B. | 石墨Ⅰ附近发生的反应:NO2-e-+NO3-═N2O5 | |
| C. | O2在石墨Ⅱ附近发生氧化反应,Y为NO | |
| D. | 相同条件下,放电过程中消耗的NO2和O2的体积比为2:1 |
15.下列有机物的系统命名正确的是( )
| A. | 2-乙基丁烷 | B. | 3,3-二甲基丁烷 | ||
| C. | 2-甲基-1,3-丁二烯 | D. | 2,2-二甲基-3-戊炔 |
5.氮化硅(Si3N4)是一种新型的耐高温耐磨材料,氮化硅属于( )
| A. | 离子晶体 | B. | 分子晶体 | C. | 金属晶体 | D. | 原子晶体 |
12.下列电离方程式错误的是( )
| A. | HCl→H++Cl- | B. | H2CO3?2H++CO32- | ||
| C. | NaCl→Na++Cl- | D. | NH3•H2O?NH4++OH- |
2.有一种活跃在中学化学题中的物质叫氢化铵(NH5).有人认为它的结构与氯化铵相似,所有的原子最外层都符合相应稀有气体原子的最外层电子层结构,与水反应有气体生成.事实上,目前为止尚未有人能够成功制取氢化铵,所以此物质是否存在仍有争议.但想法还是要有的,万一发现了呢?假设它真的存在,上述观点也正确,则下列有关说法正确的是( )
| A. | NH5中N元素的化合价是+5价 | |
| B. | 1molNH5中含有5NA个N-H键 | |
| C. | NH5的电子式为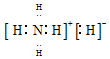 | |
| D. | NH5只由两种非金属元素组成,所以它是共价化合物 |