题目内容
8.常温下,向1LpH=10的KOH溶液中持续通入CO2,与溶液中水电离出的c(OH-)与通入的CO2的体积(V)关系如图所示.下列叙述不正确的是( )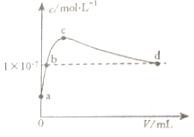
| A. | b点溶液呈中性 | |
| B. | d点溶液中:c(K+)=2c(CO32-)+c(HCO3-) | |
| C. | c点溶液中:2c(H2CO3)+c(H+)+c(HCO3-)=c(OH-) | |
| D. | a点溶液中:水电离出的c(H+)=1×10-10mol•L-1 |
分析 a点水电离出的c(OH-)最小,说明其抑制水电离程度最小,溶质为KOH;
b点KOH抑制水电离程度等于K2CO3促进水电离程度相等,则水电离出的c(OH-)=1×10-7mol•L-1,该点溶液中c(KOH)<c(K2CO3);
c点水电离程度最大,说明该点溶液中溶质为K2CO3;
d点溶液中水电离出的c(OH-)=1×10-7mol•L-1,溶液呈中性;
A.b点溶液中溶质为KOH和K2CO3,且c(KOH)<c(K2CO3);
B.d点溶液呈中性,根据电荷守恒判断;
C.c点溶液中溶质为碳酸钾,溶液中存在质子守恒,根据质子守恒判断;
D.a点为KOH溶液,水电离出的c(H+)等于溶液中c(H+).
解答 解:a点水电离出的c(OH-)最小,说明其抑制水电离程度最小,溶质为KOH;
b点KOH抑制水电离程度等于K2CO3促进水电离程度相等,则水电离出的c(OH-)=1×10-7mol•L-1,该点溶液中c(KOH)<c(K2CO3);
c点水电离程度最大,说明该点溶液中溶质为K2CO3;
d点溶液中水电离出的c(OH-)=1×10-7mol•L-1,溶液呈中性;
A.b点溶液中溶质为KOH和K2CO3,且c(KOH)<c(K2CO3),KOH是碱、碳酸钾是强碱弱酸盐,所以该溶液呈碱性,故A错误;
B.d点溶液呈中性,则c(H+)=c(OH-),根据电荷守恒得c(K+)=2c(CO32-)+c(HCO3-),故B正确;
C.c点溶液中溶质为碳酸钾,溶液中存在质子守恒,根据质子守恒得2c(H2CO3)+c(H+)+c(HCO3-)=c(OH-),故C正确;
D.a点为KOH溶液,水电离出的c(H+)等于溶液中c(H+),所以水电离出的c(H+)=10-pHmol•L-1=1×10-10mol•L-1,故D正确;
故选A.
点评 本题考查酸碱混合溶液定性判断,为高频考点,侧重考查学生分析判断能力,明确各点溶液中溶质成分及其性质是解本题关键,易错选项是A,注意b点溶液不呈中性,KOH抑制水电离程度等于碳酸钾促进水电离程度导致溶液中水电离出的c(OH-)为1×10-7mol•L-1,为易错题.

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案| A. | “84”消毒液中的NaClO有强氧化性,可杀菌消毒 | |
| B. | 使用Na2CO3溶液比使用洗涤剂淸洗餐具更环保 | |
| C. | 铝、氧化铝烧结成的金属陶瓷能耐高温、不易破碎 | |
| D. | 钙、铁、锌、铜、碘是人体必需的微量元素 |
| A. | 保存在棕色瓶中 | B. | 不易挥发 | C. | 与铜不反应 | D. | 受热不分解 |
| 弱酸 | CH3COOH | H2CO3 | HNO2 |
| 电离常数 | K=1.8×10-5 | K=4.3×10-7 K=5.6×10-11 | K=5.0×10-4 |
(1)25℃时,0.10mol•L-1Na2CO3溶液的pH=11,则溶液中由水电离出的c(OH-)=10-3
(2)常温下,将20mL0.10mol•L-1CH3COOH溶液和 20mL0.10mol•L-1HNO2 溶液分别与 20mL 0.10mol•L-1NaHCO3溶液混合(混合后溶液体积变化忽略不计).
①反应开始时,v (CH3COOH )<v (HNO2)(填“>”、“<”或“:”).
②充分反应后.两溶液中c(CH3COO-)< c(NO2-)(填“>”、“<”或“=”).
(3)25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中$\frac{c(C{H}_{3}CO{O}^{-})}{c(C{H}_{3}COOH)}$=18;
(4)常温下,下列方法可以使0.1mol•L-1CH3COOH的电离程度增大的是bc.
a.加入少量的稀盐酸
b.加热溶液
c.加水稀释
d.加入少量冰醋酸.
 )的说法错误的是( )
)的说法错误的是( )| A. | 苯乙烯与乙烯互为同系物 | B. | 所有原子可能在同一平面 | ||
| C. | 可使酸性KMnO4溶液褪色 | D. | 可发生加成反应 |
| A | B | C | D | |
| 用品名称 |  太阳能电池 |  食用油 |  84消毒液 |  合成纤维宇航服 |
| 类别或 主要成分 | SiO2 | 酯类物质 | 混合物 | 高分子材料 |
| A. | A | B. | B | C. | C | D. | D |
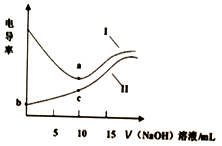 用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )
用0.1mol•L-1NaOH溶液分别滴定10mL相同浓度的盐酸和醋酸(溶质用HA表示),利用电导率传感器绘制电导率曲线如图所示.下列说法不正确的是( )| A. | b点pH值大于1 | B. | 盐酸浓度为 0.lmol•L-1 | ||
| C. | c点:c(Na+)>c(A-)>c(H+)>c(OH-) | D. | 曲线Ⅰ为盐酸,曲线Ⅱ为醋酸溶液 |
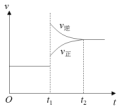 如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )
如图是工业合成氨反应的速率-时间图象,在 t1时刻改变某一条件,到 t2时重新达到平衡,判断 t1时刻可能改变条件是( )| A. | 使用催化剂 | B. | 升高温度 | C. | 增大压强 | D. | 提高 N2浓度 |