题目内容
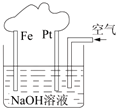 有关如图装置的叙述正确的是( )
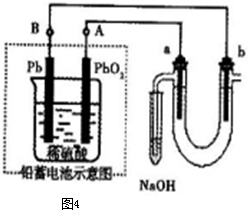
有关如图装置的叙述正确的是( )分析:该装置是铁发生的吸氧腐蚀,属于原电池,较活泼的金属铁作负极,铂作正极,负极上铁失电子生成亚铁离子,正极上氧气得电子和水反应生成氢氧根离子,外电路上电子从铁沿导线流向铂.
解答:解:A.电子从铁沿导线流向铂,故A错误;
B、该装置中铁发生吸氧腐蚀,属于原电池,故B错误;
C、该装置中铁是负极,电极反应式为:Fe-2e-+2OH-=Fe(OH)2,故C错误;
D.该装置Pt为正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应为:O2+2H2O+4e-=4OH-,故D正确.
故选D.
B、该装置中铁发生吸氧腐蚀,属于原电池,故B错误;
C、该装置中铁是负极,电极反应式为:Fe-2e-+2OH-=Fe(OH)2,故C错误;
D.该装置Pt为正极,正极上氧气得电子和水反应生成氢氧根离子,电极反应为:O2+2H2O+4e-=4OH-,故D正确.
故选D.
点评:本题以金属的腐蚀为载体考查了原电池原理,明确酸性条件下,钢铁发生析氢腐蚀,中性或碱性条件下,发生吸氧腐蚀.

练习册系列答案
相关题目
( 12分)从石器、青铜器到铁器时代,金属的冶炼体现了人类文明的发展水平。下图表示了三种金属被人类开发利用的大致年限。
(1)上述图中的三种常用金属的开发利用之所以有先后,主要取决于
(填选项序号)
| A.金属的导电性强弱 | B.金属在地壳中的含量多少 |
| C.金属的化合价高低 | D.金属的活动性大小 |
①写出"曾青得铁则化为铜"的离子方程式 。
②若根据上述反应设计成原电池,请在方框中画出原电池的装置图,标出正、负极和电解质溶液,并写出电极反应式。
正极反应
负极反应

③设计一个实验方案,使如图装置中的铁棒上析出铜,而铁的质量不变。(可用文字叙述也可用图示意)。

(3)铁路工人常用铝热反应来焊接钢轨,写出有关的化学方程式 。
教材中引发铝热反应的试剂是 。