题目内容
在含有35.8g Na2CO3和NaHCO3混合物的溶液中加入200mL 某浓度的盐酸,恰好完全反应,生成8.96L CO2(标准状况).则原溶液中有 mol Na2CO3,盐酸的物质的量浓度为 mol/L.
考点:化学方程式的有关计算
专题:计算题
分析:(1)利用n=
计算出CO2的物质的量,利用混合物的质量关系即碳原子守恒来列式计算;
(2)恰好完全反应,最后生产NaCl,由钠离子的物质的量可知盐酸中HCl的物质的量,再利用c=
计算浓度.
| V |
| Vm |
(2)恰好完全反应,最后生产NaCl,由钠离子的物质的量可知盐酸中HCl的物质的量,再利用c=
| n |
| V |
解答:
解:(1)标准状况下CO2的物质的量为
=0.4mol,
设Na2CO3和NaHCO3的物质的量分别为x、y,
由质量即碳原子守恒可知,
,解得x=0.1 mol,y=0.3 mol,
故答案为:0.1;
(2)因恰好完全反应,最后生成NaCl,
钠离子的物质的量为0.1mol×2+0.3mol=0.5mol,
由NaCl~HCl可知,HCl的物质的量为0.5mol,
则盐酸浓度为
=2.5 mol/L,
答:盐酸的物质的量浓度为2.5 mol/L.
| 8.96L |
| 22.4L/mol |
设Na2CO3和NaHCO3的物质的量分别为x、y,
由质量即碳原子守恒可知,
|
故答案为:0.1;
(2)因恰好完全反应,最后生成NaCl,
钠离子的物质的量为0.1mol×2+0.3mol=0.5mol,
由NaCl~HCl可知,HCl的物质的量为0.5mol,
则盐酸浓度为
| 0.5mol |
| 0.2L |
答:盐酸的物质的量浓度为2.5 mol/L.
点评:本题考查钠的化合物与酸的反应,明确发生的化学反应和产物,利用守恒法即可快速解答.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
被称之为“软电池”的纸质电池,采用一个薄层纸片(在其一边镀锌,而在其另一边喷涂二氧化锰)作为传导体.在纸内的离子“流过”水和氧化锌组成的电解液.电池总反应为Zn+2Mn02+H2O=ZnO+2MnO(OH),下列说法正确的是( )
| A、该电池的负极为锌,工作时锌离子向负极移动 |
| B、该电池反应中二氧化锰起氧化剂作用 |
| C、当0.1mol Zn完全溶解时,转移电子个数为1.204×1024 |
| D、电池负极反应式为:2Mn02+2e-+2H2O=2MnO(OH)+2OH- |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、标准状况下,11.2LNH3和11.2LHCl混合后分子总数为NA |
| B、标准状况下,22.4LSO2与11.2LO2在催化剂作用下反应,一定生成NA个SO3分子 |
| C、标准状况下,在100ml 2mol?L-1H2SO4溶液中加入足量Na2SO3稀溶液,可收集到0.2NA个SO2气体分子 |
| D、1molFe2+ 与足量的H2O2溶液反应,转移NA个电子 |
关于下列图示的说法中正确的( )
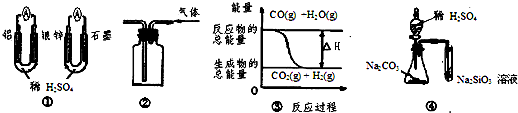

| A、图 ①两个装置中通过导线的电子数相同时,消耗负极材料的物质的量也相同 |
| B、用图 ②所示实验装置排空气法收集CO2气体 |
| C、图 ③表示可逆反应“CO(g)+H2O(g)?CO2(g)+H2(g)”为吸热反应 |
| D、用图 ④所示实验可比较硫、碳、硅三种元素的非金属性强弱 |
少量钠应保存在( )
| A、密闭容器中 | B、水中 |
| C、煤油中 | D、四氯化碳中 |
 如图是以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下:
如图是以Zn和Cu为电极,稀硫酸为电解质溶液形成的原电池,某实验兴趣小组做完实验后,在读书卡片上记录如下: 化学在能源开发与利用中起着十分关键的作用.
化学在能源开发与利用中起着十分关键的作用.