题目内容
某化学兴趣小组拟采用下图装置甲电解饱和氯化钠溶液,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量Ar(Cu),同时检验氯气的氧化性,图中夹持和加热仪器已略去.
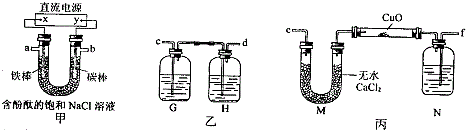
(1)写出装置甲中反应的离子方程式: .
(2)为完成上述实验,正确的连接顺序为a连 ,b连 (填写连接的字母).
(3)装置乙中第一个广口瓶内的溶液不能是( )
A、淀粉碘化钾溶液 B、NaOH溶液 C、FeCl3与KSCN混合溶液 D、Na2SO3溶液
(4)在对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为 .
(5)装置丙中广口瓶内盛放的试剂为 ,作用是 .
(6)为了测定Cu的相对原子质量,某同学通过实验测得丙装置反应前后如下数据:样品质量为m1g,反应后硬质玻璃管中剩余固体质量为m2g,反应前后U型管及其中固体质量为m3g,反应前后洗气瓶及其中液体质量差为m4g.
①请选择理论上误差最小的一组数据计算Ar(Cu).Ar(Cu)= .
②如果选用其他组数据进行计算,会导致Ar(Cu) (填“偏大”、“偏小”或“不受影响”).理由是 .

(1)写出装置甲中反应的离子方程式:
(2)为完成上述实验,正确的连接顺序为a连
(3)装置乙中第一个广口瓶内的溶液不能是( )
A、淀粉碘化钾溶液 B、NaOH溶液 C、FeCl3与KSCN混合溶液 D、Na2SO3溶液
(4)在对硬质玻璃管里的氧化铜粉末加热前,需进行的操作为
(5)装置丙中广口瓶内盛放的试剂为
(6)为了测定Cu的相对原子质量,某同学通过实验测得丙装置反应前后如下数据:样品质量为m1g,反应后硬质玻璃管中剩余固体质量为m2g,反应前后U型管及其中固体质量为m3g,反应前后洗气瓶及其中液体质量差为m4g.
①请选择理论上误差最小的一组数据计算Ar(Cu).Ar(Cu)=
②如果选用其他组数据进行计算,会导致Ar(Cu)
考点:电解原理,氯气的化学性质
专题:
分析:(1)根据电解原理,与阴极相连的是外接电源的负极;甲中电解饱和食盐水;
(2)“通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu)”故a接f;“同时检验Cl2的氧化性”,故b接c;
(3)A、D中的I-、SO32-都有还原性,但是Cl2与SO32-反应没有现象;氯气有毒,不能直接排放到空气中,氯气可以用碱性物质来处理,C中FeCl3和KSCN溶液不能证明氯气的氧化性;
(4)氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,所以加热氧化铜之前要通入氢气排净装置内的空气(或检验H2的纯度防止爆炸);
(5)电解饱和氯化钠溶液制备的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选浓硫酸干燥H2,防止硬质试管炸裂;
(6)①CuO+H2=Cu+H2O△m=80-64=16,现在质量差为m1-m2,而“反应后硬质玻璃管中剩余固体质量为m2g”,即Cu的质量为m2g.根据化学方程式就可求出Ar(Cu);
②空气中的水通过e导管进入U型管造成m3增大,最终导致Ar(Cu)偏小.
(2)“通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu)”故a接f;“同时检验Cl2的氧化性”,故b接c;
(3)A、D中的I-、SO32-都有还原性,但是Cl2与SO32-反应没有现象;氯气有毒,不能直接排放到空气中,氯气可以用碱性物质来处理,C中FeCl3和KSCN溶液不能证明氯气的氧化性;
(4)氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,所以加热氧化铜之前要通入氢气排净装置内的空气(或检验H2的纯度防止爆炸);
(5)电解饱和氯化钠溶液制备的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选浓硫酸干燥H2,防止硬质试管炸裂;
(6)①CuO+H2=Cu+H2O△m=80-64=16,现在质量差为m1-m2,而“反应后硬质玻璃管中剩余固体质量为m2g”,即Cu的质量为m2g.根据化学方程式就可求出Ar(Cu);
②空气中的水通过e导管进入U型管造成m3增大,最终导致Ar(Cu)偏小.
解答:
解:(1)根据电解原理,与阴极相连的是外接电源的负极,故X极应为负极;甲中电解饱和食盐水,反应的离子方程式为2Cl-+2H2O
2OH-+H2↑+Cl2↑,
故答案为:2Cl-+2H2O
2OH-+H2↑+Cl2↑;
(2)“通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu)”故a接f;“同时检验Cl2的氧化性”,故b接c,故答案为:f;c;
(3)A、D中的I-、SO32-都有还原性,但是Cl2与SO32-反应没有现象,FeCl3与KSCN混合溶液和氯气不反应,不能证明氯气的氧化性,故选BCD;氯气有毒,不能直接排放到空气中,氯气可以用碱性物质来处理,所以装置乙瓶中H中液体的作用是吸收多余的氯气,防止环境污染;
故答案为:BCD;
(4)氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,所以加热氧化铜之前要通入氢气排净装置内的空气(或检验H2的纯度防止爆炸).故答案为:检验氢气的纯度防止爆炸;
(5)通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),但由于电解饱和氯化钠溶液制备的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选浓硫酸,干燥H2,防止硬质试管炸裂;
故答案为:浓硫酸;干燥H2,防止硬质试管炸裂;
(6)①由CuO→Cu知△m=80-64=16,现在质量差为m1-m2,而“反应后硬质玻璃管中剩余固体质量为m2g”,即Cu的质量为m2g.根据化学方程式则
CuO+H2=Cu+H2O△m Ar(Cu) 16
m2 m1-m2
解得Ar(Cu)=
;
故答案为:
;
②空气中的水通过e导管进入U型管造成m3增大,
CuO+H2=Cu+H2O
Ar(Cu)+16 18
m1 m3
Ar(Cu)=
-16,
m3增大导致Ar(Cu)减小;
故答案为:偏小;空气中的水通过e导管进入U型管造成m3增大,最终导致Ar(Cu)偏小.
| ||
故答案为:2Cl-+2H2O
| ||
(2)“通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu)”故a接f;“同时检验Cl2的氧化性”,故b接c,故答案为:f;c;
(3)A、D中的I-、SO32-都有还原性,但是Cl2与SO32-反应没有现象,FeCl3与KSCN混合溶液和氯气不反应,不能证明氯气的氧化性,故选BCD;氯气有毒,不能直接排放到空气中,氯气可以用碱性物质来处理,所以装置乙瓶中H中液体的作用是吸收多余的氯气,防止环境污染;
故答案为:BCD;
(4)氢气是可燃性气体,与氧气混合,加热容易发生爆炸危险,所以加热氧化铜之前要通入氢气排净装置内的空气(或检验H2的纯度防止爆炸).故答案为:检验氢气的纯度防止爆炸;
(5)通过H2还原氧化铜测定Cu的相对原子质量Ar(Cu),但由于电解饱和氯化钠溶液制备的氢气中含有水蒸气,所以在实验前要除去水蒸气,故选浓硫酸,干燥H2,防止硬质试管炸裂;
故答案为:浓硫酸;干燥H2,防止硬质试管炸裂;
(6)①由CuO→Cu知△m=80-64=16,现在质量差为m1-m2,而“反应后硬质玻璃管中剩余固体质量为m2g”,即Cu的质量为m2g.根据化学方程式则
CuO+H2=Cu+H2O△m Ar(Cu) 16
m2 m1-m2
解得Ar(Cu)=
| 16m2 |
| m1-m2 |
故答案为:
| 16m2 |
| m1-m2 |
②空气中的水通过e导管进入U型管造成m3增大,
CuO+H2=Cu+H2O
Ar(Cu)+16 18
m1 m3
Ar(Cu)=
| 18m1 |
| m3 |
m3增大导致Ar(Cu)减小;
故答案为:偏小;空气中的水通过e导管进入U型管造成m3增大,最终导致Ar(Cu)偏小.
点评:本题考查电解原理应用、氯气检验、氢气还原氧化铜实验操作、元素相对原子质量的测定的实验设计等,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
对于某些离子的检验及结论一定正确的是( )
| A、加入稀盐酸产生无色无味气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32? |
| B、加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42? |
| C、加入氯水后再加入KSCN溶液,溶液变红色,一定有Fe2+ |
| D、加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+ |
常温下可盛放浓硫酸的容器是( )
| A、Na | B、Zn | C、Al | D、Mg |
加强食品检测是保证食品安全、保护公众利益的重要举措.下列一般不属于食品安全检测指标的是( )
| A、氯气 | B、二氧化硫 |
| C、亚硝酸钠 | D、碘酸钾 |
已知氯化银在水中存在沉淀溶解平衡:AgCl?Ag++Cl-,现将足量的氯化银分别放入下列选项的溶液中,充分搅拌后,相同温度下,银离子浓度最小的是( )
| A、100mL蒸馏水中 |
| B、50mL0.1mol?L-1的氯化镁溶液 |
| C、150mL0.1mol?L-1的氯化钠溶液 |
| D、50mL0.1mol?L-1的氯化铝溶液 |