题目内容
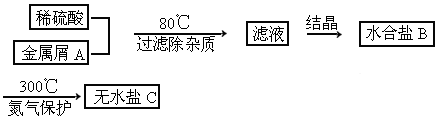
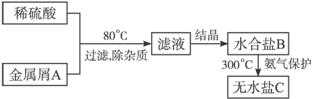
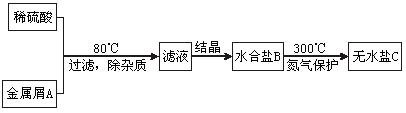
下图表示某种盐的制备步骤:
已知:水合盐B含有45.3%的水;无水盐C焙烧分解,放出两种无色刺激性气体E和F,并生成红棕色固体D.
请写出物质的化学式或名称:
A____ ____,B__ ______,C_____ ___,D____ ____,E___ _____,F____ ____.
短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5.X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物.请回答:
(1)X元素的名称是________;Y元素的名称是________;Z元素的名称是________.
(2)XZ3化合物的化学式是________________,电子式是________________.
(3)分别写出X、Y的含氧酸的化学式________、________.
答案:
解析:
提示:
解析:
| Fe FeSO4·7H2O FeSO4 Fe2O3 SO2 SO3(或SO3 SO2)
|
提示:
| 阅读全题后,找到解题的突破口:红棕色固体D为Fe2O3;由此确定金属A为Fe;Fe与稀H2SO4反应生成FeSO4,根据“水合盐B含有45.3%的水”,确定B为FeSO4·7H2O.(设含结晶水为x, 做此类试题不仅要注意突破口的寻找,还一定要注意思维的缜密.如“水合盐B在300℃、氮气保护”下得到无水盐C.虽说“氮气保护”在课堂的学习中很少出现,但引起重视即可发现这便是防止氧化的措施,必为亚铁盐.另外只有C为FeSO4,才能从氧化还原的角度上确认两种无色刺激性气体,即
|

练习册系列答案
相关题目
 .若为
.若为