题目内容
已知:N2(g)+3H2(g)2SO3(g)(正反应为放热反应)。
请回答下列问题:
(1)从影响化学反应速率和化学平衡的因素分析,要有利于NH3和SO3的生成,理论上应采取的措施是_________。实际生产中采取的措施是_________。
(2)在合成氨的工业生产中,要分离出氨,目的是_________;而合成SO3的过程中,不要分离出SO3,原因是_________。
解析:工业上合成SO3与合成氨的最大不同之处是该反应是在常压下进行的,原因是在常压下该反应向生成SO3的方向进行程度已经很大,采用高压虽能使平衡向生成SO3方向移动,但产生高压既需要动力又对反应容器耐压性有较高要求,综合生产成本和经济效益两方面因素,实际生产时,在常压下进行最合理。
答案:(1)高温、高压、催化剂 合成氨:高温、高压、催化剂;合成SO3:高温、常压、催化剂
(2)减小生成物的浓度,使平衡向生成NH3的方向移动 该反应向生成SO3的方向进行程度较大,达到平衡后SO2剩余量较少,故不需要分离SO3

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
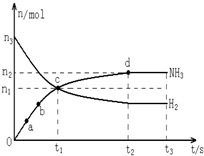 自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题:
自1913年工业合成氨投产以来,合成氨工业不断发展,氨又可以进一步制备硝酸,在工业上可进行连续生产.请回答下列问题: