题目内容
向一定量的Fe2O3和Fe的混合物中加50mL 2mol?L-1 H2SO4,在一定条件下恰好使混合物完全溶解,并放出224mL(标准状况)的气体,在所得溶液中加入KSCN溶液,无红色出现,那么混合物中铁的质量为多少克?
考点:有关混合物反应的计算
专题:计算题
分析:在所得溶液中加入KSCN溶液,无红色出现,说明反应生成了硫酸亚铁,根据硫酸的物质的量可知硫酸亚铁的物质的量;标况下224mL气体为氢气,其物质的量为:
=0.01mol,铁与稀硫酸反应生成0.01mol氢气的同时会生成0.01mol硫酸亚铁,据此可以计算出铁与铁离子反应生成的亚铁离子的物质的量,从而得出 混合物中铁的总质量.
| 0.224L |
| 22.4L/mol |
解答:
解:反应后的溶液中加入KSCN溶液,无红色出现,说明反应生成了硫酸亚铁,根据硫酸根守恒可知:n(FeSO4)=n(H2SO4)=0.05L×2mol/L=0.1mol,
标况下224mL气体为氢气,其物质的量为:
=0.01mol,根据反应Fe+H2SO4=FeSO4+H2↑可知,则生成0.01mol氢气时会生成0.01molFeSO4,消耗铁的物质的量为:n(Fe)=n(H2)=0.01mol,
反应2Fe3++Fe=3Fe2+生成的FeSO4的物质的量为:0.1mol-0.01mol=0.09mol,则该反应中消耗铁的物质的量为:n(Fe)=0.09mol×
=0.03mol,
所以原混合物中铁的总物质的量为:0.01mol+0.03mol=0.04mol,质量为:56g/mol×0.4mol=22.4g,
答:混合物中铁的质量为22.4g.
标况下224mL气体为氢气,其物质的量为:
| 0.224L |
| 22.4L/mol |
反应2Fe3++Fe=3Fe2+生成的FeSO4的物质的量为:0.1mol-0.01mol=0.09mol,则该反应中消耗铁的物质的量为:n(Fe)=0.09mol×
| 1 |
| 3 |
所以原混合物中铁的总物质的量为:0.01mol+0.03mol=0.04mol,质量为:56g/mol×0.4mol=22.4g,
答:混合物中铁的质量为22.4g.
点评:本题考查了有关混合物反应的计算,题目难度中等,明确题干信息及发生反应的原理为解答关键,注意质量守恒定律在化学计算中的应用方法,试题侧重考查学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
下列反应的方程式书写正确的( )
A、氯乙烷消去反应制乙烯:CH3CH2Cl
| |||
B、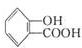 +2Na2CO3→ +2Na2CO3→ +2NaHCO3 +2NaHCO3 | |||
| C、苯酚钠溶液中通入少量二氧化碳:2C6H5O-+CO2+H2O→2C6H5OH+CO32- | |||
D、甲醛溶液中加入足量的银氨溶液并水浴加热:HCHO+2[Ag(NH3)2]+2OH-
|
在密闭容器中有可逆反应:nA(g)+mB(g)?pC(g)△H>0处于平衡状态,(已知m+n>p),则下列说法正确的是:①升温,
的比值变小②降温时体系内混合气体平均分子量变小③加入B,A的转化率增大④加入催化剂,气体总的物质的量不变⑤加压使容器体积减小,A或B的浓度一定降低⑥若A的反应速率为VA,则B的反应速率为
( )
| c(B) |
| c(C) |
| n?VA |
| m |
| A、①②③⑤ | B、①②③④ |
| C、①②⑤⑥ | D、③④⑤⑥ |
下列原理或用途不正确的是( )
| A、酒精消毒是对蛋白的变性作用 |
| B、天然皮革是变性蛋白质 |
| C、误食重金属盐会使人中毒,可以服用鸡蛋清帮助解毒 |
| D、坏血病患者应该多吃的食物是鱼肉和猪肉 |
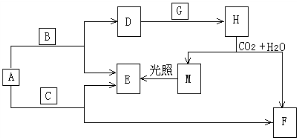
 已知:A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料.
已知:A是来自石油的重要有机化工原料,此物质可以用来衡量一个国家石油化工发展水平.E是具有果香味的有机物,F是一种高聚物,可制成多种包装材料.
 已知25℃、101kPa下,氢气、甲烷和葡萄糖的燃烧热依次为285.8kJ/mol、890.3kJ/mol、2800kJ/mol.
已知25℃、101kPa下,氢气、甲烷和葡萄糖的燃烧热依次为285.8kJ/mol、890.3kJ/mol、2800kJ/mol.