题目内容
7.由铜、锌和稀硫酸组成的原电池中,正极是铜,电极反应是2H++2e-=H2↑;负极是锌,电极反应是Zn-2e-=Zn2+.分析 原电池形成条件是活泼性不同的两个电极,电解质溶液,闭合回路,自发进行的氧化还原反应,原电池中,较活泼金属作负极,负极失电子发生氧化反应,另一极作正极,正极得电子发生还原反应.
解答 解:由铜、锌和稀硫酸组成的原电池中,锌较活泼做负极失电子发生氧化反应,电极反应为Zn-2e-=Zn2+;铜做正极,溶液中氢离子得到电子生成氢气,发生还原反应,电极反应为2H++2e-=H2↑,铜极表面产生气泡;
故答案为:铜,2H++2e-=H2↑;锌,Zn-2e-=Zn2+.
点评 本题考查原电池的正负极的判断及电极反应式,注意根据氧化还原反应得失电子判断原电池的正负极,题目较简单.

练习册系列答案
相关题目
18.下列实验现象与对应化学方程式都正确的是( )
| A. | 金属钠投入水中,浮在水面熔成小球,并在水面快速移动,得到的溶液显碱性;2 Na+2 H2O═2 NaOH+H2↑ | |
| B. | 氢气在氯气中安静的燃烧,发出淡蓝色火焰,瓶口出现白雾;H2+Cl2$\frac{\underline{\;点燃\;}}{\;}$2HCl | |
| C. | FeSO4溶液中加入NaOH溶液时,生成的白色絮状沉淀迅速变为灰绿色,最后变成红褐色; 2Fe(OH)2+O2+H2O═2 Fe(OH)3 | |
| D. | 向Na2SiO3溶液中逐滴加入稀盐酸,边加边振荡,有透明的硅酸凝胶产生;Na2SiO3+2HCl═H2SiO3(胶体)+2NaCl |
2.下列说法不正确的是( )
| A. | 化学反应达到化学平衡状态的正逆反应速率相等,是指同一物质的消耗速率和生成速率相等,若用不同物质表示时,反应速率不一定相等 | |
| B. | 标准状况下,1 L辛烷完全燃烧生成CO2 8 L | |
| C. | 2.4 g Mg无论与O2还是与N2完全反应,转移电子数都是0.2NA | |
| D. | 1 L 1 mol•L-1 CH3COOH溶液中,所含CH3COO-、CH3COOH的总数为NA |
12.反应A(g)+3B(g)═2C(g)+2D(g),在不同情况下测得反应速率,其中反应速率最快的是( )
| A. | v(A)=0.4mol/(L•s) | B. | v(B)=0.5mol/(L•s) | C. | v(C)=0.6mol/(L•s) | D. | v(D)=0.7mol/(L•s) |
19.下列有关说法正确的是( )
| A. | 常温下,向醋酸溶液中加入少量的水,溶液中c(H+)将增大 | |
| B. | 常温下,2NO(g)+2CO(g)?N2(g)+2CO2(g)能自发进行,则该反应的△H<0 | |
| C. | 硫酸铜饱和溶液降低温度时有晶体析出,可用熵判据来解释 | |
| D. | 用CH3COOH溶液做导电实验,灯泡很暗,一定能证明CH3COOH是弱电解质 |
17.下列各组离子中,能在强酸性溶液中能大量共存的是( )
| A. | Na+、K+、Ca2+、HCO3- | B. | OH-、Cl-、Na+、NH${\;}_{4}^{+}$ | ||
| C. | Cu2+、Na+、SO42-、Cl- | D. | Mg2+、Na+、Cl-、CH3COO- |
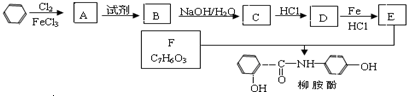
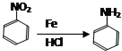
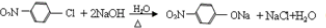 .
.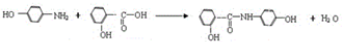 .
. .
.