题目内容
7.氯胺是由氯气遇到氧气反应生成的一类化合物,是常用的饮用水二级消毒剂,主要包括一氯胺(NH2CL)、二氣胺(NHC12)和三氯胺(NC13).氯胺消毒时首先发生水解,生成具有强烈杀菌作用的次氯酸.(1)HH2C1中氯元素的化合价为+1 ,其电子式为
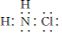 .
.(2)NH2C1水解的离子方程式为NH2Cl+2H2O?NH3•H2O+HClO
(3)三氯胺在常温下为黄色黏稠的油状液体,有毒,在弱酸性溶液中稳定性较好,将0.01NCL3通入100mL 0.5mol•L-1 Na2SO4溶液中,转移电子的物质的量为0.06 mol.
(4)已知:
2NH3 (g)+3Cl2 (g) N2(g)+6HCl(g)△H1=-469kJ•mol-1
N2(g)+3C12(g) 2NC13(g)△H2=+520kJ•mol-1
NH3(g)十3Cl2 (g) NCl3 (g)+3HCL(g)△H3则△H3=+25.5kJ•mol-1.
分析 (1)根据化合价的代数和为0计算;NH2Cl是共价化合物,N、Cl原子周围8个电子;
(2)NH2Cl水解生成一水合氨和HClO;
(3)NCl3中Cl元素的化合价为+1价,反应生成Cl为-1价,结合物质的量计算;
(4)己知:①2NH3(g)+3C12(g)=N2(g)+6HCl(g)△H1=-469kJ/mol
②N2(g)+3C12(g)=2NC13(g)△H2=+520kJ/mol,根据盖斯定律,$\frac{1}{2}$(①+②)得到NH3(g)+3C12(g)=NC13(g)+3HCl(g)据此计算.
解答 解:(1)NH2Cl中N元素为-3价,H为+1价,则氯元素的化合价为+1价;NH2Cl是共价化合物,N、Cl原子周围8个电子,则其电子式为: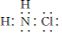 ;
;
故答案为:+1;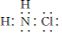 ;
;
(2)NH2Cl水解生成一水合氨和HClO,水解方程式为NH2Cl+2H2O?NH3•H2O+HClO;
故答案为:NH2Cl+2H2O?NH3•H2O+HClO;
(3)NCl3中Cl元素的化合价为+1价,反应生成Cl为-1价,0.01mol NCl3转移电子为0.06mol,100mL0.5mol/LNa2SO3溶液中Na2SO3为0.05mol,Na2SO3作还原剂能失去0.1mol电子,所以Na2SO3过量,按照NCl3计算转移电子为0.06mol;
故答案为:0.06mol;
(4)己知:①2NH3(g)+3C12(g)=N2(g)+6HCl(g)△H1=-469kJ/mol,
②N2(g)+3C12(g)=2NC13(g)△H2=+520kJ/mol,
根据盖斯定律,$\frac{1}{2}$(①+②)得到NH3(g)+3C12(g)=NC13(g)+3HCl(g),则△H3=$\frac{1}{2}$(-469kJ/mol++520kJ/mol)=+25.5kJ/mol;
故答案为:+25.5.
点评 本题考查氧化还原反应、盖斯定律的计算,为高频考点,把握反应中元素的化合价变化以及盖斯定律的内容为解答的关键,注意从化合价角度分析氧化还原反应,难度中等.

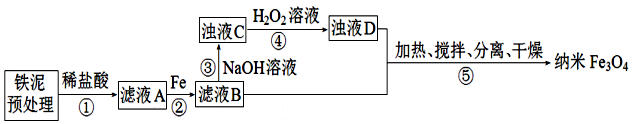
已知:步骤⑤中,相同条件下测得Fe3O4的产率与R(R=$\frac{n(\stackrel{+3}{Fe})}{n(\stackrel{+2}{Fe})}$)的关系如图所示.
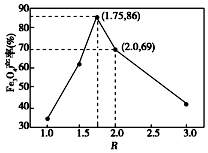
(1)为提高步骤①的反应速率,可采取的措施是搅拌、适当升高温度.
(2)步骤②中,主要反应的离子方程式是2Fe3++Fe=3Fe2+.
(3)常温下Fe3+、Fe2+以氢氧化物形式完全沉淀时溶液的pH如图.该温度下Ksp[Fe(OH)3]=1.0×10-38
| 沉淀物 | Fe(OH)3 | Fe(OH)2 |
| 完全沉淀物PH | 3.0 | 8.3 |
步骤④中,反应完成后需再加热一段时间除去剩余H2O2目的是加热使其分解除去,防止其在步骤⑤中继续氧化+2价铁元素
(5)⑤反应的离子方程式为2FeOOH+Fe2++2OH-$\frac{\underline{\;\;△\;\;}}{\;}$Fe3O4+2H2O;步骤⑤中的“分离”包含的步骤有过滤、洗涤.
(6)设浊液D中FeOOH的物质的量为a,滤液B中的铁元素的物质的量为b.为使Fe3O4的产率最高,则$\frac{a}{b}$=0.636.(填数值,小数点后保留3位)
| A. | SO2为0.8mol/L,O2为0.4 mol/L | B. | SO2为0.5 mol/L | ||
| C. | SO3为0.8 mol/L | D. | SO2、SO3均为0.3 mol/L |
| A. | 醋酸纤维属于酯类 | |
| B. | 顺-2-丁烯与反-2-丁烯的沸点不同 | |
| C. | 脱氧核糖核酸(DNA)是高分子有机物 | |
| D. | 由苯酚与溴水的反应可知,苯环影响了羟基 |
| A. | 2H2O?H3O++OH- | B. | H2S?H++HS- | C. | NaHS=Na++HS- | D. | HCO3-=H++CO32- |
| A. | 1molFeCl3与沸水反应生成胶体后,含有NA个Fe(OH)3胶粒 | |
| B. | 25℃、1.01×105 Pa下,44g CO2中含有的原子数为3NA | |
| C. | 1 L 0.5mol/L Na2CO3 溶液中含有的CO32-数目为0.5NA | |
| D. | 1 mol Cl2与足量Fe反应,转移的电子数为3NA |
| A. | 在5min内该反应用C的浓度变化表示的反应速率为0.2mol/(L•min) | |
| B. | 5min时,容器内D的浓度为0.2mol/L | |
| C. | 当容器内压强保持恒定时,该可逆反应达到平衡状态 | |
| D. | 5min时容器内气体总的物质的量为3mol |
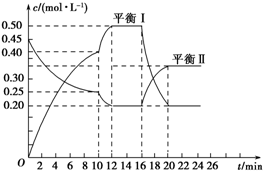 向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)?yC(g)△H<0
向一容积不变的密闭容器中充入一定量A和B,发生如下反应:xA(g)+2B(s)?yC(g)△H<0