题目内容
图表中评价合理的是
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | 向氢氧化亚铁溶液中加入足量的稀硝酸:Fe(OH)2+2H+=Fe2++2H2O | 正确 |
| B | 用食醋除去水瓶中的水垢:C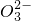 +2CH3COOH→2CH3COO-+CO2↑+H2O +2CH3COOH→2CH3COO-+CO2↑+H2O | 错误,水垢的主要成分碳酸钙,不应写成离子形式 |
| C | 向明矾溶液中加入过量的氢氧化钡溶液:Al3++S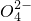 +Ba2++4OH-=BaSO4↓+Al +Ba2++4OH-=BaSO4↓+Al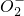 +2H2O +2H2O | 正确 |
| D | 用铂电极电解氯化钡溶液:Cl-+2H2O=Cl2↑+H2↑+OH- | 正确 |
- A.A
- B.B
- C.C
- D.D
B
分析:A、稀硝酸具有强氧化性能氧化亚铁离子;
B、水垢成分为碳酸钙难溶于水;
C、量少的不符合化学式组成比;
D、电解氯化钡,阳极氯离子放电,阴极是氢离子放电.
解答:A、向氢氧化亚铁溶液中加入足量的稀硝酸具有氢氧化性,反应的离子方程式为3Fe(OH)2+NO3-+10H+=3Fe3++8H2O+NO↑,故A错误;
B、用食醋除去水瓶中的水垢反应的离子方程式为CaCO3+2CH3COOH→2CH3COO-+CO2↑+H2O+Ca2+,故B正确;
C、向明矾溶液中加入过量的氢氧化钡溶液,反应的离子方程式为Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故C错误;
D、电解氯化钡,阳极氯离子放电,阴极是氢离子放电,所以生成氯气、氢气和氢氧化钡,反应的离子方程式为2Cl-+2H2O=Cl2↑+H2↑+2OH-,故D错误;
故选B.
点评:本题考查了离子方程式的书写方法和注意问题,注意量不同产物不同,氧化性物质发生的氧化还原反应,电解原理应用,题目难度中等.
分析:A、稀硝酸具有强氧化性能氧化亚铁离子;
B、水垢成分为碳酸钙难溶于水;
C、量少的不符合化学式组成比;
D、电解氯化钡,阳极氯离子放电,阴极是氢离子放电.
解答:A、向氢氧化亚铁溶液中加入足量的稀硝酸具有氢氧化性,反应的离子方程式为3Fe(OH)2+NO3-+10H+=3Fe3++8H2O+NO↑,故A错误;
B、用食醋除去水瓶中的水垢反应的离子方程式为CaCO3+2CH3COOH→2CH3COO-+CO2↑+H2O+Ca2+,故B正确;
C、向明矾溶液中加入过量的氢氧化钡溶液,反应的离子方程式为Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O,故C错误;
D、电解氯化钡,阳极氯离子放电,阴极是氢离子放电,所以生成氯气、氢气和氢氧化钡,反应的离子方程式为2Cl-+2H2O=Cl2↑+H2↑+2OH-,故D错误;
故选B.
点评:本题考查了离子方程式的书写方法和注意问题,注意量不同产物不同,氧化性物质发生的氧化还原反应,电解原理应用,题目难度中等.

练习册系列答案
 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案
相关题目
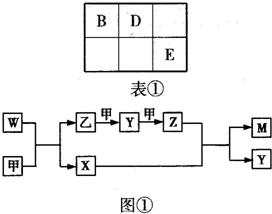 A、B、D、E四种元素均为短周期元素,原子序数逐渐增大.A元素原子的核外电子数、电子层数和最外层电子数均相等.B、D、E三种元素在周期表中相对位置如表①所示,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子中含有10个电子.它们之间的转化关系如图①所示.
A、B、D、E四种元素均为短周期元素,原子序数逐渐增大.A元素原子的核外电子数、电子层数和最外层电子数均相等.B、D、E三种元素在周期表中相对位置如表①所示,只有E元素的单质能与水反应生成两种酸.甲、乙、M、W、X、Y、Z七种物质均由A、B、D三种元素中的一种或几种组成,其中只有M分子同时含有三种元素;W为A、B两元素组成的18电子分子,可作火箭燃料;甲、乙为非金属单质;X分子中含有10个电子.它们之间的转化关系如图①所示. 如图是化学实验室某试剂瓶标签上的部分内容.下列相关叙述错误的是
如图是化学实验室某试剂瓶标签上的部分内容.下列相关叙述错误的是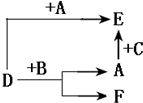 A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是
A、B、C分别是三种常见单质;D、E、F则是常见的三种氧化物,且有如图所示转化关系,下列说法错误的是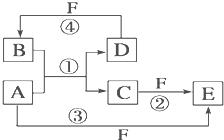 A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).
A、B、C、D、E、F六种物质的转化关系如图所示(反应条件和部分产物未标出).