题目内容
17.下列有关Cl、N、S等非金属元素化合物的说法正确的是( )| A. | 漂白粉的主要成分为次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 实验室可用NaOH溶液处理NO2和HCl废气 | |
| D. | 它们对应的含氧酸都是强酸 |
分析 A.氯气与石灰乳反应制备漂白粉;
B.浓硫酸与氨气反应;
C.NO2和HCl均与NaOH反应;
D.HClO、亚硝酸、亚硫酸等均为弱酸,而高氯酸、硝酸、硫酸为强酸.
解答 解:A.氯气与石灰乳反应制备漂白粉,主要成分为氯化钙、次氯酸钙,有效成分为次氯酸钙,故A错误;
B.浓硫酸与氨气反应,则不能利用浓硫酸干燥氨气,故B错误;
C.NO2和HCl均与NaOH反应,则实验室可用NaOH溶液处理NO2和HCl废气,故C正确;
D.HClO、亚硝酸、亚硫酸等均为弱酸,而高氯酸、硝酸、硫酸为强酸,则它们对应的含氧酸不都是强酸,故D错误;
故选C.
点评 本题考查非金属及化合物的性质,为高频考点,把握物质的性质、发生的反应为解答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
7.下列化合物中不可能通过化合反应制得的是( )
①Fe(OH)3②FeCl2③Fel3④SO3⑤CuS⑥NaHCO3.
①Fe(OH)3②FeCl2③Fel3④SO3⑤CuS⑥NaHCO3.
| A. | ③⑤⑥ | B. | ③④⑤⑥ | C. | ③⑤ | D. | ②③⑤ |
8.N2O5是一种新型硝化剂,在一定温度下可发生如下反应:2N2O5(g)?4NO2(g)+O2(g)△H>0.T1温度时,向密闭容器中通入N2O5气体,部分实验数据见下表:
下列说法正确的是( )
| 时间/s | 0 | 500 | 1000 | 1500 |
| c(N2O5)/(mol•L-1) | 5.00 | 3.52 | 2.50 | 2.50 |
| A. | 500 s内NO2的生成速率为2.96×10-3 mol•L-1•s-1 | |
| B. | T1温度下该反应平衡时N2O5的转化率为29.6% | |
| C. | 达到平衡其他条件不变,将容器的体积压缩到原来1/2,则c(N2O5)<5.00mol•L-1 | |
| D. | T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1>K2 |
12.说法正确的是( )
| A. | 若1mol Na2O2与足量水反应后产生氧气,理论上转移的电子数为2×6.02×1023 | |
| B. | 0.1mol/L Na2CO3溶液加热后,溶液的pH减小 | |
| C. | 室温下稀释0.1mol/L CH3COOH溶液,溶液的导电能力减弱,因此溶液中所有离子浓度均减小 | |
| D. | 向废水中滴加FeCl3饱和溶液制备Fe(OH)3胶体的原理是加热促进Fe3+水解 |
2.下列说法正确的是( )
| A. | 某物质不属电解质,就属于非电解质 | |
| B. | SO3溶于水可导电,SO3属于电解质 | |
| C. | 能导电的物质属于电解质,NaCl属于电解质,NaCl晶体可导电 | |
| D. | 已知氧化铝在熔融状态下能导电,则氧化铝在熔融状态下能电离 |
16.下列文字表述与反应方程式对应且正确的是( )
| A. | 溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+=AgBr↓ | |
| B. | 少量CO2气体通入苯酚钠溶液中:2 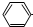 →O-+H2O+CO2→2 →O-+H2O+CO2→2 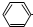 -OH+CO32- -OH+CO32- | |
| C. | 甲苯与浓硝酸和浓硫酸的混合物反应: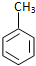 +3HNO3$→_{100℃}^{浓H_{2}SO_{4}}$ +3HNO3$→_{100℃}^{浓H_{2}SO_{4}}$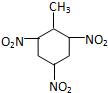 +3H2O +3H2O | |
| D. | 工业上通过苯与乙烯反应获得乙苯: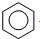 +CH2═CH2$→_{△}^{催化剂}$ +CH2═CH2$→_{△}^{催化剂}$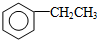 |
 实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯 ②100mL量筒 ③容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码)
实验室用固体NaOH配制0.5mol/L的NaOH溶液500mL,有以下仪器和用品有:①烧杯 ②100mL量筒 ③容量瓶 ④药匙 ⑤玻璃棒 ⑥托盘天平(带砝码)
 .
.