题目内容
11.重铬酸盐广泛用作氧化剂、皮革制作等.以铬矿石(主要成分是Cr2O3,含FeO、Al2O3、SiO2等杂质)为原料制取重铬酸钠的流程如下: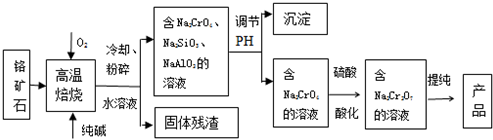
请回答下列问题:
(1)写出:Cr2O3与纯碱在高温焙烧时反应的化学方程式2Cr2O3+4Na2CO3+3O2$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+4CO2,Na2CrO4用硫酸酸化时反应的离子方程式2CrO42-+2H+Cr2O72-+H2O;
(2)Na2Cr2O7可用于测定废水的化学耗氧量(即COD,指每升水样中还原性物质被氧化所需要O2的质量).现有某水样100.00mL,酸化后加入C1 mol/L的Na2Cr2O7溶液 V1 mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用C2mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL.
①该水样的COD为480C1V1-80C2V2mg/L;
②假设上述反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1mol/L,要使Fe3+沉淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是3.2~4.3之间,(可能用到的数据:KSPFe(OH)3=4.0×10-38,KSPCr(OH)3=6.0×10-31,lg$\root{3}{0.4}$=-0.1,lg$\root{3}{4}$=0.2,lg$\root{3}{6}$=0.3,lg$\root{3}{60}$=0.6)
(3)在Na2Cr2O7溶液中加入固体KC1进行复分解反应即可制得橙色的K2Cr2O7,请分析此反应能发生的原因K2Cr2O7的溶解度小于Na2Cr2O7的溶解度,加入固体KCl时使K2Cr2O7超饱和而析出晶体.
(4)酸性的K2Cr2O7溶液常用于酒驾的检验,写出反应的离子方程式2Cr2O72-+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O,反应时可观察到的现象是溶液由橙色变为绿色.
分析 以铬矿石(主要成分是Cr2O3,含FeO、Al2O3、SiO2等杂质)为原料,加入碳酸钠和氧气高温灼烧发生反应生成铬酸钠,二氧化碳,水浸后过滤得到滤渣FeO,滤液为Na2CrO4,Na2SiO3,NaAlO2;调节溶液PH沉淀硅酸跟离子和偏铝酸根离子,过滤得到滤液Na2CrO4,加入硫酸酸化生成重铬酸钠溶液,通过提纯得到重铬酸钠.
(1)铬矿石中加入碳酸钠和氧气高温灼烧发生反应生成铬酸钠,二氧化碳,依据原子守恒和电子守恒配平写出化学方程式;硫酸酸化使Na2CrO4转化为Na2Cr2O7,依据电荷守恒写出离子方程式;
(2)①根据题意废水与K2Cr2O7溶液发生氧化还原反应,再用Fe2+把多余的Cr2O72-反应:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,则与废水反应反应的K2Cr2O7的物质的量=加入的K2Cr2O7的物质的量-与Fe2+反应的K2Cr2O7的物质的量,利用2K2Cr2O7~3O2可求出废水中化学耗氧量即COD;
②铁离子完全沉淀的浓度为10-5mol/L,铬离子不沉淀的浓度为0.1mol/L,由溶度积常数计算溶液氢氧根离子浓度,结合离子积常数换算氢离子浓度计算得到溶液pH;
(3)K2Cr207的溶解度小于Na2Cr207的溶解度,根据溶解度大的物质能转化为溶解度小的物质解答;
(4)酸性的K2Cr207溶液常用于酒驾的检验,铬元素化合价+6价降低到+3价,碳元素化合价升高从-2价升高为0价,据此书写离子反应方程式;Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇,现象据此解答.
解答 解:(1)由图示可知Cr2O3在高温焙烧时生成Na2CrO4,发生氧化还原反应,反应的化学方程式为:2Cr2O3+4Na2CO3+3O2$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+4CO2,在酸性环境下,CrO42-转化为Cr2O72-,在酸性环境下,CrO42-转化为Cr2O72-,即2CrO42-+2H+Cr2O72-+H2O,
故答案为:2Cr2O3+4Na2CO3+3O2$\frac{\underline{\;高温\;}}{\;}$4Na2CrO4+4CO2;2CrO42-+2H+Cr2O72-+H2O;
(2)①样品100.00mL,酸化后加入c1mol/L的Na2Cr2O7溶液 V1mL,使水中的还原性物质完全被氧化(Cr2O72-还原为Cr3+);再用4mol/L的FeSO4溶液滴定剩余的Cr2O72-,结果消耗FeSO4溶液V2mL,废水与K2Cr2O7溶液发生氧化还原反应,再用Fe2+把多余的Cr2O72-反应:
Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,
1 6
n C2mol/L×V2×10-3L
则:n=$\frac{{C}_{2}{V}_{2}}{6}$×10-3mol,
则100ml废水中,与废水反应反应的K2Cr2O7的物质的量=加入的K2Cr2O7的物质的量-与Fe2+反应的K2Cr2O7的物质的量=c1mol/L×V1×10-3L-$\frac{{C}_{2}{V}_{2}}{6}$×10-3mol,
1L废水水样中被还原的K2Cr2O7的物质的量=(c1V1-$\frac{{C}_{2}{V}_{2}}{6}$)×10-2mol,
利用2K2Cr2O7~3O2可求出废水中化学耗氧量即COD,
2 K2Cr2O7 ~3 O2
2 3×32
(c1V1-$\frac{{C}_{2}{V}_{2}}{6}$)×10-2mol m
则:m=(48c1V1-8c2V2)×10-2g=(480c1V1-80c2V2)mg,该水样的COD为:(480c1V1-80c2V2)mg/L,
故答案为:480C1V1-80C2V2;
②反应后所得溶液中Fe3+和Cr3+的物质的量浓度均为0.1mol/L,要使Fe3+沉 淀完全而Cr3+还未开始沉淀,需要c(Fe3+)=10-5mol/l时铁离子沉淀完全,由溶度积常数Ksp=c(Fe3+)c3(OH-),c3(OH-)=$\frac{4.0×1{0}^{-38}}{1×1{0}^{-5}}$=4.0×10-33,c(OH-)=$\root{3}{4}$×10-11mol/L,c(H+)=$\frac{1{0}^{-14}}{\root{4}{4}×1{0}^{-11}}$=10-3.2,pH=-lgc(H+)=3.2;
Cr3+还未开始沉淀,c(Cr3+)=0.1mol/L,Ksp=c(Cr3+)c3(OH-)=6.0×10-31,c3(OH-)=$\frac{6.0×1{0}^{-31}}{0.1}$=6.0×10-30;c(OH-)=$\root{3}{6}$×10-10mol/L,c(H+)=$\frac{1{0}^{-14}}{\root{3}{6}×1{0}^{-10}}$=10-4.3mol/L,pH=-lgc(H+)=4.3,
则要使Fe3+沉淀完全而Cr3+还未开始沉淀.则需调节溶液pH的范围是3.2~4.3,
故答案为:3.2~4.3之间;
(3)由于K2Cr2O7的溶解度小于Na2Cr2O7的溶解度,则加入固体KCl时发生反应:Na2Cr2O7+2KCl=K2Cr2O7↓+2NaCl,使K2Cr2O7超饱和而析出晶体,
故答案为:K2Cr2O7的溶解度小于Na2Cr2O7的溶解度,加入固体KCl时使K2Cr2O7超饱和而析出晶体;
(4)酸性的K2Cr2O7溶液常用于酒驾的检验,铬元素化合价+6价降低到+3价,碳元素化合价升高从-2价升高为0价,根据质量守恒定律和得失电子守恒原理,反应为:2Cr2O72-+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O,Cr2O72-和Cr3+在溶液中分别显橙色和绿色,可利用颜色的变化检验乙醇,即橙色的Cr2O72-在酒精作用下转化为绿色的Cr3+,则能检查司机是否酒后开车,所以反应时可观察到的现象是溶液由橙色变为绿色,
故答案为:2Cr2O72-+3C2H5OH+16H+=4Cr3++3CH3COOH+11H2O;溶液由橙色变为绿色.
点评 本题考查了滴定实验的计算、沉淀溶解平衡的溶度积常数计算的相关知识,题目难度较大,注意把握滴定原理以及实验的过程分析,明确实验目的、实验原理为解答关键,试题培养了学生的分析能力及化学实验能力.

 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案| A. | 2CH3CH2OH+O2$→_{△}^{催化剂}$2CH3CHO+2H2O | |
| B. | 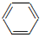 +HO-Na2$→_{60℃}^{浓硫酸}$ +HO-Na2$→_{60℃}^{浓硫酸}$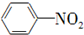 +H2O +H2O | |
| C. | CH2═CH2+H2O$\stackrel{催化剂}{→}$CH3-CH2OH | |
| D. | CH3COOCH2CH3+NaOH$\stackrel{△}{→}$CH3COONa+CH3CH2OH |
②2Na(s)+O2(g)=Na2O2(s)△H=-511kJ.mol-1
下列说法不正确的是( )
| A. | ①和②产物的阴阳离子个数比相等 | |
| B. | ①和②生成等物质的量的产物,转移电子数相同 | |
| C. | 常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 | |
| D. | 25℃、101kPa下:Na2O2(s)+2Na(s)=2Na2O(s)△H=-317kJ.mol-1 |
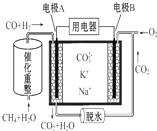
| A. | CH4+H2O$\frac{\underline{\;催化剂\;}}{△}$3 H2+CO,1 mol CH4参加反应转移12 mol电子 | |
| B. | 电极A为正极 | |
| C. | 电池工作时,CO32-向电极B移动 | |
| D. | O2在B电极上被还原 |
| A. | 0.1mol•L-1的NaOH溶液中含Na+数目为0.1NA | |
| B. | 标准状况下,2.24L乙酸中含碳原子数目为0.2NA | |
| C. | 12gC60中含质子总数为6NA | |
| D. | 0.1molCl2与足量NaOH溶液反应,转移电子数目为0.2NA |
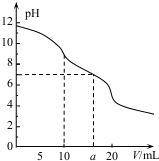 常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )
常温下,用 0.1mol•L HCl溶液滴定10.0mL浓度为0.1mol•L-1 Na2CO3溶液,所得滴定曲线如图所示.下列说法正确的是( )| A. | 当V=0时:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-) | |
| B. | 当V=5时:c(Na+ )>c(HCO3-)>c(CO32- )>c(Cl- ) | |
| C. | 当V=a时:c(Na +)>c(Cl- )>c(H+ )=c(OH- ) | |
| D. | 当V=10时:c(H+ )+c(H2CO3)=c(OH- )+c(CO32-) |
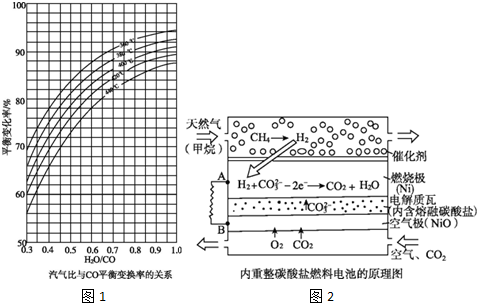
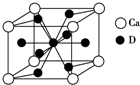 A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题:
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大.第二周期元素A原子的核外成对电子数是未成对电子数的2倍且有3个能级,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素.D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满.请回答下列问题: