题目内容
试管中盛有白色晶体,检验它是不是铵盐的方法中不可行的是( )
| A、加热,将湿润的红色石蕊试纸放在管口 |
| B、加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口 |
| C、加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口 |
| D、加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在管口 |
考点:铵离子检验
专题:
分析:A.氯化铵在试管底部受热分解,在试管口重新反应生成氯化铵;
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口,观察是否产生能使试纸变红的气体;
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口,观察是否冒白烟;
D.铵根离子与碱反应生成氨气,氨气具有碱性,能使湿润的红色石蕊试纸变蓝.
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口,观察是否产生能使试纸变红的气体;
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口,观察是否冒白烟;
D.铵根离子与碱反应生成氨气,氨气具有碱性,能使湿润的红色石蕊试纸变蓝.
解答:
解:A.若铵盐为氯化铵,氯化铵在试管底部受热分解,在试管口重新反应生成氯化铵,无法检验氨气,故A错误;
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口,观察是否产生能使试纸变红的气体,故B正确;
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口,观察是否冒白烟,故C正确;
D.铵根离子与碱反应生成氨气,氨气具有碱性,能使湿润的红色石蕊试纸变蓝,故D正确;
故选:A.
B.加氢氧化钠溶液,加热,将湿润的酚酞试纸放在管口,观察是否产生能使试纸变红的气体,故B正确;
C.加氢氧化钠溶液,加热,将蘸有浓盐酸的玻璃棒放在管口,观察是否冒白烟,故C正确;
D.铵根离子与碱反应生成氨气,氨气具有碱性,能使湿润的红色石蕊试纸变蓝,故D正确;
故选:A.
点评:本题考查了铵盐的检验方法,题目难度不大,根据课本知识即可解答.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
下列表示对应化学反应的离子方程式正确的是( )
| A、NaHSO4溶液与Ba(OH)2溶液反应至中性:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O |
| B、向40 mL 8 mol/L的稀硝酸溶液中加入5.6 g铁粉:Fe+4H++NO3-=Fe3++NO↑+2H2O |
| C、用稀硝酸洗涤试管内壁的银镜:Ag+2H++NO3-=Ag++NO↑+H2O |
| D、FeI2溶液中通入过量Cl2:2Fe2++2I-+2Cl2=2Fe3++I2+4Cl- |
根据原子结构与元素周期律的知识,下列推断正确的是( )
| A、同主族元素含氧酸的酸性随核电荷数的增加而减弱 |
| B、核外电子排布相同的微粒化学性质也相同 |
| C、Cl-、S2-、Ca2+、K+半径逐渐减小 |
| D、1735 Cl 与 1737 Cl 得电子能力相同 |
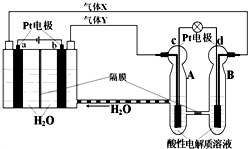 RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图.下列有关说法正确的是( )
RFC是一种将水电解技术与氢氧燃料电池技术相结合的可充电电池,RFC工作原理见图.下列有关说法正确的是( )| A、转移0.1mol电子时,a电极产生标准状况下O21.12L |
| B、b电极上发生的电极反应是:2H2O+2e-=H2↑+2OH- |
| C、c电极上进行还原反应,B池中的H+可以通过隔膜进入A池 |
| D、d电极上发生的电极反应是:O2+4H++4e-=2H2O |
被称之为“软电池”的纸质电池总反应为Zn+2MnO2+H2O=ZnO+2MnOOH.下列说法正确的是( )
| A、该电池中Zn作负极,发生还原反应 |
| B、该电池反应中MnO2起催化作用 |
| C、该电池工作时电流由Zn经导线流向MnO2 |
| D、该电池正极反应式为:MnO2+e-+H2O=MnOOH+OH- |