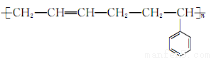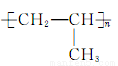题目内容
在硫酸铁电化浸出黄铜矿精矿工艺中,有一主要反应:CuFeS2+4Fe3+===Cu2++5Fe2++2S,反应结束后,经处理获得单质硫x mol。下列说法正确的是( )
A.反应中硫元素被氧化,所有铁元素均被还原
B.氧化剂是Fe3+,氧化产物是Cu2+
C.反应中转移电子的物质的量为x mol
D.反应结束后,测得溶液中三种金属离子的总物质的量为y mol,则原Fe3+的总物质的量为(y-x)mol
D
【解析】
试题分析:A、反应中S元素的化合价由-2价升高为0价,被氧化,反应物中的Fe元素有+2、+3价,+3价的Fe被还原,所以不是全部的Fe元素被还原,错误;B、铁离子被还原,作氧化剂,S元素被氧化,所以氧化产物是S单质,错误;C、S的物质的量是xmol,则转移电子的物质的量是2xmol,错误;D、单质硫的物质的量是xmol,则溶液中Cu2+的物质的量是0.5xmol,Fe2+的物质的量是2.5xmol,此时溶液中未反应的Fe3+的物质的量是y-0.5x-2.5x=(y-3x)mol,已反应的Fe3+的物质的量是2x,所以原溶液y-3x+2x=(y-x)mol,答案选D。
考点:考查氧化还原反应的分析与计算

 名校课堂系列答案
名校课堂系列答案下列是某同学对相应的离子方程式所作的评价,其中评价合理的是
编号 | 化学反应 | 离子方程式 | 评 价 |
A | 碳酸钙与醋酸反应 | CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- | 错误,碳酸钙是弱电解质,不应写成离子形式 |
B | 苯酚钠溶液中通入CO2 | 2C6H5O-+CO2+H2O→2C6H5OH+CO32- | 正确 |
C | NaHCO3的水解 | HCO3-+H2O═CO32-+H3O+ | 错误,水解方程式误写成电离方程式 |
D | 等物质的量的FeBr2和Cl2反应 | 2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- | 错误,离子方程式中Fe2+与Br-的物质的量之比与化学式不符 |
 数目为0.2NA
数目为0.2NA 的溶液:K+、Ba2+、NO3-、AlO-2
的溶液:K+、Ba2+、NO3-、AlO-2 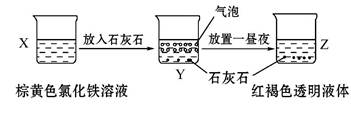
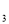 +2Fe3++3H
+2Fe3++3H O====2Fe(OH)3+3CO
O====2Fe(OH)3+3CO ↑+3Ca2+
↑+3Ca2+ +3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓
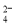

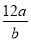 B.m g该氯原子的物质的量是
B.m g该氯原子的物质的量是 mol
mol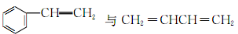 制高聚物
制高聚物