��Ŀ����
9����1���������������������£���ʼ���������ʵ���[��n��H2����ʾ]��N2��g��+3H2��g��?2NH3��g����Ӧ��Ӱ��ɱ�ʾ����ͼ1��ʾ�Ĺ��ɣ�ͼ��t��ʾ�¶ȣ�n��ʾ���ʵ��������ٱȽ���a��b��c���㴦��ƽ��״̬�У���Ӧ��N2��ת������ߵ���C��
���������ݻ�Ϊ1L��n=3mol����Ӧ�ﵽƽ��ʱH2��ת����Ϊ60%��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ1mol���������£�t2����Ӧ��ƽ�ⳣ��K=2.08��mol/L��-2��ͼ����t2��t1�Ĺ�ϵ��t2���� t1������ڡ������ڡ������ڡ�����ȷ��������
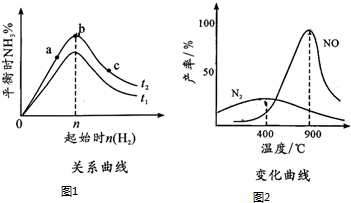
��2��������������145��ʱ��ʼ��Ӧ���ڲ�ͬ�¶Ⱥʹ������������ɲ�ͬ�����ͼ2��ʾ��
4NH3+5O2?4NO+6H2O
4NH3+3O2?2N2+6H2O
�¶Ƚϵ�ʱ������N2Ϊ�����¶ȸ���900��ʱ��NO�����½���ԭ���ǰ�����������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½���N2��g��+O2��g��=2NO��g����H=+��b-a��/2 kJ•mol-1��
���� ��1��������ʱ�¶���ͬ��������Խ������ת����Խ��
�ڸ�������ʽ���K=$\frac{��������ƽ��Ũ��ϵ������֮��}{������Ӧ��ƽ��Ũ��ϵ������֮��}$���м��㣻
����ͼ��֪������������ͬʱ��T1�ȴﵽƽ����ƽ��ʱ������Ũ��С��
��2������ͼ���֪�¶ȵ�ʱ���ɵ������¶ȸ�ʱ����NO�����÷�ӦΪ���ȷ�Ӧ�����¶ȸ���900��ʱ��NO�����½���������������ԭ����д�Ȼ�ѧ����ʽ��
��� �⣺��1��������ʱ�¶���ͬ��������Խ������ת����Խ����c���ת������ߣ��ʴ�Ϊ��C��
��N2��g��+3H2��g��?2NH3��g��
��ʼ x 3 0
ת��0.6 1.8 1.2
ƽ��x-0.6 1.2 1.2
N2��ת����Ϊ60%����$\frac{0.6}{x}$��100%=60%�����x=1mol��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ1mol����Ӧ��ƽ�ⳣ��K=$\frac{1��{2}^{2}}{0.4��1��{2}^{3}}$=2.08��mol/L��-2��
�ʴ�Ϊ��1��2.08��mol/L��-2��
����ͼ��֪������������ͬʱ��T1�ȴﵽƽ����ƽ��ʱ������Ũ��С����T2����T1���ʴ�Ϊ�����ڣ�
��2������ͼ���֪�¶ȵ�ʱ���ɵ������¶ȸ�ʱ����NO�����÷�ӦΪ���ȷ�Ӧ�����¶ȸ���900��ʱ��NO�����½���
��֪��4NH3��g��+5O2��g��?4NO��g��+6H2O��l����H=-a kJ•mol-1
��4NH3��g��+3O2��g��?2N2��g��+6H2O ��l����H=-b kJ•mol-1
����-�ڣ���2�ã�N2��g��+O2��g��=2NO��g����H=+��b-a��/2 kJ•mol-1
�ʴ�Ϊ��N2��������������NO�ķ�Ӧ�Ƿ��ȷ�Ӧ�������¶�ת�����½���N2��g��+O2��g��=2NO��g����H=+��b-a��/2 kJ•mol-1��
���� ���⿼��������ͼ��ķ����Լ�����������ԭ����ƽ����йؼ���ȣ���Ŀ�Ѷ��еȣ�

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| A�� | �÷�Ӧ���ڷֽⷴӦ | B�� | ͼ�е����ֻ����ﶼ���������� | ||
| C�� | �÷�Ӧ��Ԫ�صĻ��ϼ�û�б仯 | D�� | ��Ӧǰ��ԭ�ӵ�����ı� |
 ��ij�ݻ�һ�����ܱ������У����淴Ӧ��A��g��+B��g���TxC��g����ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ���˵������ȷ���ǣ�T��ʾ�¶ȣ�p��ʾѹǿ��C%��ʾC�������������������
��ij�ݻ�һ�����ܱ������У����淴Ӧ��A��g��+B��g���TxC��g����ͼ����ʾ�ķ�Ӧ���ߣ����ж϶�ͼ���˵������ȷ���ǣ�T��ʾ�¶ȣ�p��ʾѹǿ��C%��ʾC�������������������| A�� | p3��p4��y���ʾA�����ʵ��� | |
| B�� | p3��p4��y���ʾB��������� | |
| C�� | p3��p4��y���ʾ���������ܶ� | |
| D�� | p3��p4��y���ʾ��������ƽ����Է������� |
 �����仯�����ڹ�ҵ���������������й㷺Ӧ�ã��ش��������⣺
�����仯�����ڹ�ҵ���������������й㷺Ӧ�ã��ش��������⣺��1�����������ȶ��������������������õ���ʽ��ʾ�������γɹ��̣�
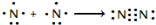 ��
����2��������N2H4����һ�ֻ�ԭ������֪��H2O��l���TH2O��g����H=+44kJ/mol���Խ���±����ݣ�д��N2H4 ��g��ȼ���ȵ��Ȼ�ѧ����ʽ��N2H4��g��+O2��g��=N2��g��+2H2O��l����H=-631.7kJ/mol��
| ��ѧ�� | N-H | N-N | N�TN | N��N | O�TO | O-H |
| ���ܣ�kJ/mol�� | 390.8 | 193 | 418 | 946 | 497.3 | 462.8 |
��4�����Ĵ��������ڹ�ҵ�������ᣮ�÷�Ӧ����Ƴ����͵�أ���д�����Ի����£��õ�صĸ����缫��Ӧʽ��NH3-5e-+5OH-=NO+4H2O��
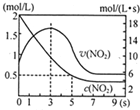
��5����ijŨ�ȵ�NO2�������һ���ݾ��������У�������Ӧ2NO2?N2O4�����ͼ����ͼ��
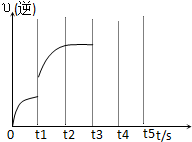
��0��3sʱv��NO2�������ԭ��������Ϊ������ϵ���÷�Ӧ������з��ȣ���ϵ�¶����ߣ�v��NO2������
��5sʱNO2ת����Ϊ75%��
CH3CH2CH2CH3��g��+$\frac{13}{2}$O2��g���T4CO2��g��+5H2O��l����H=-2 878kJ/mol
��CH3��2CHCH3��g��+$\frac{13}{2}$O2��g���T4CO2��g��+5H2O��l����H=-2 869kJ/mol
����˵����ȷ���ǣ�������
| A�� | 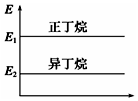 ���������춡���������С��ϵ��ͼ | |
| B�� | ��������ȶ��Դ����춡�� | |
| C�� | �춡��ת��Ϊ������Ĺ�����һ�����ȹ��� | |
| D�� | �춡������е�̼�����������Ķ� |
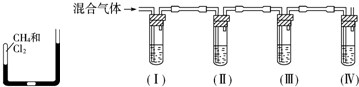
 �п��淴Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g������֪938Kʱƽ�ⳣ��K=1.47��1173Kʱƽ�ⳣ��K=2.15��
�п��淴Ӧ��Fe��s��+CO2��g��?FeO��s��+CO��g������֪938Kʱƽ�ⳣ��K=1.47��1173Kʱƽ�ⳣ��K=2.15�� ��֪KMnO4��MnO2�����������¾��ܽ����� ��H2C2O4��������
��֪KMnO4��MnO2�����������¾��ܽ����� ��H2C2O4��������