题目内容
下列说法中正确的是( )
| A、过渡元素包括d、ds、f共三个区的元素,共中d区元素共包括六列六族 |
| B、在分子中碳原子形成双键,则该碳原子一定采取sp2杂化 |
| C、已知N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g),若该反应中有4 mol N-H键断裂,则形成的π键有2mol |
| D、植物光合作用所需的叶绿素是一种镁的配合物 |
考点:原子轨道杂化方式及杂化类型判断,元素周期表的结构及其应用
专题:
分析:A.d区包含8列;
B.在分子中碳原子形成双键,则该碳原子不一定采取sp2杂化;
C.N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g),若该反应中有4 mol N-H键断裂,则有1mol肼参加反应,生成1.5mol氮气,每个氮气分子中含有2个π键;
D.植物光合作用所需的叶绿素是一种镁的配合物,镁原子和N原子之间形成配位键.
B.在分子中碳原子形成双键,则该碳原子不一定采取sp2杂化;
C.N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g),若该反应中有4 mol N-H键断裂,则有1mol肼参加反应,生成1.5mol氮气,每个氮气分子中含有2个π键;
D.植物光合作用所需的叶绿素是一种镁的配合物,镁原子和N原子之间形成配位键.
解答:
解:A.过渡元素包括d、ds、f共三个区的元素,共中d区元素共包括8列6族,故A错误;
B.在分子中碳原子形成双键,则该碳原子不一定采取sp2杂化,如二氧化碳中C原子采用sp杂化,故B错误;
C.N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g),若该反应中有4 mol N-H键断裂,则有1mol肼参加反应,生成1.5mol氮气,每个氮气分子中含有2个π键,所以若该反应中有4 mol N-H键断裂,则形成的π键有3mol,故C错误;
D.植物光合作用所需的叶绿素是一种镁的配合物,为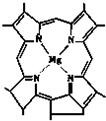 ,镁原子和N原子之间形成配位键,故D正确;
,镁原子和N原子之间形成配位键,故D正确;
故选D.
B.在分子中碳原子形成双键,则该碳原子不一定采取sp2杂化,如二氧化碳中C原子采用sp杂化,故B错误;
C.N2O4(l)+2N2H4(l)═3N2(g)+4H2O(g),若该反应中有4 mol N-H键断裂,则有1mol肼参加反应,生成1.5mol氮气,每个氮气分子中含有2个π键,所以若该反应中有4 mol N-H键断裂,则形成的π键有3mol,故C错误;
D.植物光合作用所需的叶绿素是一种镁的配合物,为
 ,镁原子和N原子之间形成配位键,故D正确;
,镁原子和N原子之间形成配位键,故D正确;故选D.
点评:本题考查较综合,涉及配合物、原子杂化、元素周期表结构等知识点,明确配位键的形成条件、价层电子对互斥理论、元素周期表结构特点即可解答,易错选项是B.

练习册系列答案
 新思维寒假作业系列答案
新思维寒假作业系列答案
相关题目
关于溴乙烷与NaOH的乙醇溶液反应说法正确的是( )
| A、该反应是溴乙烷的水解反应 |
| B、往反应后的溶液中直接加入AgNO3溶液检验是否有Br-生成 |
| C、该反应产物中有水、钠盐和不饱和烃 |
| D、生成的气体可直接通入到溴水中检验是否有乙烯生成 |
PM2.5是指大气中直径接近于2.5×10-6 m的颗粒物,下列有关PM2.5说法不正确的是( )
| A、PM2.5表面积大能吸附大量的有毒、有害物质 |
| B、PM2.5在空气中形成气溶胶 |
| C、实施绿化工程,可以有效地防治PM2.5污染 |
| D、研制开发燃料电池汽车,降低机动车尾气污染,某种程度上可以减少PM2.5污染 |
下列变化需要加入还原剂才能实现的转化是( )
| A、Fe2+→Fe3+ |
| B、H2SO4→SO2 |
| C、H2S→SO2 |
| D、HCO3-→CO2 |
向饱和CuSO4溶液中加入白色无水CuSO4粉末,表现出的现象是( )
| A、溶液质量增加 |
| B、溶液质量减少 |
| C、出现蓝色晶体 |
| D、溶液质量不变 |
已知:①向KMnO4溶液中滴加浓盐酸,产生黄绿色气体; ②向KBr溶液中通入少量实验①产生的气体,溶液变黄色; ③取实验②生成的溶液少量滴在FeCl2与KSCN的混合溶液中,溶液变血红色.根据以上实验,下列判断正确的是( )
| A、上述实验中,共有两个氧化还原反应 |
| B、上述实验证明还原性:Fe2+>Br->Cl->Mn2+ |
| C、实验①生成的气体不能使湿润的淀粉KI试纸变蓝 |
| D、实验③证明Fe2+既有氧化性又有还原性 |
 电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题: