题目内容
1.中和相同体积、相同pH的硫酸、盐酸和醋酸三种稀溶液,所用相同浓度的NaOH溶液的体积分别为V1、V2、V3,则三者的大小关系为( )| A. | V3>V2>V1 | B. | V3=V2>V1 | C. | V3>V2=V1 | D. | V1=V2>V3 |
分析 等pH的硫酸、盐酸和醋酸三种酸溶液,硫酸和氯化氢为强电解质,溶液中氢离子浓度相等,而醋酸为弱电解质,溶液中部分电离,则醋酸的浓度大于溶液中氢离子浓度,据此进行判断V1、V2、V3的关系.
解答 解:等pH的硫酸、盐酸和醋酸三种酸溶液,硫酸和氯化氢为强电解质,溶液中氢离子浓度相等,而醋酸为弱电解质,溶液中部分电离,则醋酸的浓度大于溶液中氢离子浓度,所以等体积,需要氢氧化钠的物质的量最多的是醋酸,盐酸与硫酸相等,则三者的大小关系为V3>V2=V1,故选C.
点评 本题考查了酸碱混合的定性判断及溶液中氢离子、氢氧根离子与溶液pH的关系,题目难度中等,注意掌握溶液酸碱性与溶液的pH的关系,明确弱电解质部分电离是解答本题关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列说法正确的是( )
| A. | 按系统命名法 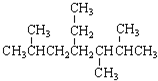 ,的名称为2,5,6-三甲基-4-乙基庚烷 ,的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 麦芽糖与蔗糖的水解产物均含葡萄糖,故二者均为还原型二糖 | |
| D. | 苯酚为无色晶体,常因为氧化呈粉红色 |
16.ClO2是一种杀菌消毒效率高、二次污染小的水处理剂.实验室中可通过以下反应制得:2KClO3+H2C2O4+H2SO4=2ClO2↑+K2SO4+2CO2↑+2H2O.下列说法不正确的是( )
| A. | 反应中有3molH2C2O4被还原,转移6mol电子 | |
| B. | KClO3发生了还原反应 | |
| C. | KClO3的还原性强于CO2的还原性 | |
| D. | ClO2作水处理剂时,利用了其强氧化性 |
13.下列关于有机物的说法中,正确的是( )
| A. | 塑料、橡胶和纤维一定都是合成高分子材料 | |
| B. | 蔗糖不是高分子化合物,其水解产物能发生银镜反应 | |
| C. | 某烃类的混合气体跟Cl2混合光照,有油状液滴生成,说明混合气体肯定含有甲烷 | |
| D. |  分子中所有原子不可能都共平面. 分子中所有原子不可能都共平面. |
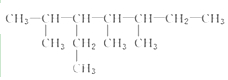 ;
;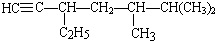 的系统名称为5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷.
的系统名称为5,6-二甲基-3-乙基-1-庚烯,将其在催化剂存在条件下完全氢化,所得烷烃的系统名称为2,3-二甲基-5-乙基-庚烷.