题目内容
13.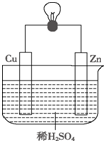 如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,做了如下记录,其中描述合理的是( )①Zn为正极,Cu为负极;
②H+向负极移动;
③电子流动方向:从Zn经外电路流向Cu;
④Cu极上有H2产生;
⑤正极的电极反应式为:Zn-2e-═Zn2+
⑥若有1mol电子流过导线,则产生H2为0.5mol.
| A. | ①②③ | B. | ③④⑥ | C. | ④⑤⑥ | D. | ②③④ |
分析 Zn-Cu原电池中,Zn作负极,发生电池反应Zn+2H+=Zn2++H2↑,电子由负极流向正极,阳离子向正极移动,以此来解答.
解答 解:①Zn-Cu原电池中,Zn失电子为负极,Cu为正极,故①错误;
②阳离子向正极反应,则H+向正极移动,故②错误;
③电子从负极流向正极,即电子由Zn电极流向Cu电极,故③正确;
④Cu电极上氢离子得电子生成氢气,即发生2H++2e-=H2↑,故④正确;
⑤正极上氢离子得电子生成氢气,则正极反应为2H++2e-=H2↑,故⑤错误;
⑥由2H++2e-=H2↑可知,有1mol电子流向导线,产生氢气0.5mol,故⑥正确;
故选B.
点评 本题考查原电池,明确电极的判断、发生的电极反应、电子、离子的移动方向即可解答,题目难度不大.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
8.具有下列电子层结构的原子,则下列有关比较中正确的是( )
①3p轨道上只有一对成对电子的原子
②外围电子构型为2s22p5的原子
③其3p轨道为半充满的原子
④正三价的阳离子结构与氖相同的原子.
①3p轨道上只有一对成对电子的原子
②外围电子构型为2s22p5的原子
③其3p轨道为半充满的原子
④正三价的阳离子结构与氖相同的原子.
| A. | 第一电离能:②>③>①>④ | B. | 原子半径:④>③>②>① | ||
| C. | 电负性:②>③>①>④ | D. | 最高正化合价:②>③>①>④ |
5.下列属于同位素的一组是( )
| A. | O2、O3 | B. | Na2O、Na2O2 | ||
| C. | ${\;}_{19}^{40}$K、${\;}_{20}^{40}$Ca | D. | ${\;}_{1}^{1}$H ${\;}_{1}^{2}$H ${\;}_{1}^{3}$H |
3.某主族元素X的电子式为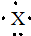 ,则该元素组成的以下物质中,化学式肯定错误的是( )
,则该元素组成的以下物质中,化学式肯定错误的是( )
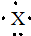 ,则该元素组成的以下物质中,化学式肯定错误的是( )
,则该元素组成的以下物质中,化学式肯定错误的是( )| A. | 含氧酸的化学式可能为HXO3 | B. | 含氧酸的化学式可能为H3XO4 | ||
| C. | 气态氢化物化学式为XH5 | D. | 最高价氧化物的化学式为X2O5 |
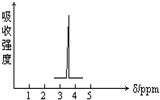 化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为:BrCH2CH2Br,请预测B的核磁共振氢谱上有2个峰(信号),强度之比为3:1.
化合物A和B的分子式都是C2H4Br2,A的核磁共振氢谱图如图所示,则A的结构简式为:BrCH2CH2Br,请预测B的核磁共振氢谱上有2个峰(信号),强度之比为3:1.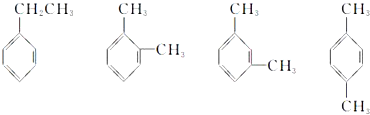

 也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是
也可与Ⅲ发生类似反应③的反应生成有机物Ⅴ.Ⅴ的结构简式是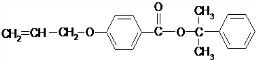 .
.