题目内容
14.下列叙述正确的是( )| A. | 使用催化剂能够降低化学反应的反应热(△H) | |
| B. | 金属发生吸氧腐蚀时,被腐蚀的速率与氧气浓度无关 | |
| C. | 原电池中发生的反应达平衡时,该电池仍有电流产生 | |
| D. | 在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小 |
分析 A.催化剂能降低反应的活化能从而改变反应速率,但不改变化学平衡;
B.金属发生吸氧腐蚀时,氧气浓度越大,腐蚀的速率越快;
C.原电池中发生的反应达平衡时,各组分浓度不再改变,电子转移总量为0,该电池无电流产生;
D.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小.
解答 解:A.催化剂能降低反应的活化能从而改变反应速率,但不改变化学平衡,则不能改变反应的反应热,故A错误;
B.金属发生吸氧腐蚀时,氧气浓度越大,腐蚀的速率越快,故B错误;
C.原电池中发生的反应达平衡时,各组分浓度不再改变,电子转移总量为0,该电池无电流产生,故C错误;
D.在同浓度的盐酸中,ZnS可溶而CuS不溶,说明CuS的溶解度比ZnS的小,故D正确.
故选D.
点评 本题考查了催化剂对化学反应的影响、金属的腐蚀及溶解度大小的比较,注意催化剂不能改变化学平衡,题目难度中等.

练习册系列答案
相关题目
11.下列关于离子共存或离子反应的说法正确的是( )
| A. | 某无色溶液中可能大量存在H+、Cl-、MnO4- | |
| B. | pH=2的溶液中可能大量存在Na+、NH4+、SiO32- | |
| C. | Fe2+与H2O2在酸性溶液中的反应:2Fe2++H2 O2+2H+═2Fe3++2H2O | |
| D. | 稀硫酸与Ba(OH)2溶液的反应:H++SO42-+Ba2++OH-═BaSO4↓+2H2O |
17.常温下,下列四种溶液中,H+浓度之比(①:②:③:④)是( )
①pH=1的醋酸溶液;②0.01mol•L-1的盐酸;③pH=11的氨水;④0.01mol•L-1的NaOH溶液.
①pH=1的醋酸溶液;②0.01mol•L-1的盐酸;③pH=11的氨水;④0.01mol•L-1的NaOH溶液.
| A. | 1:10:100:1000 | B. | 1011:1010:10:1 | C. | 1:10:1010:1011 | D. | 14:13:2:3 |
2.下列有关500mL0.2mol•L-1氨水的叙述,正确的是( )
| A. | 含有0.1molNH3•H2O | |
| B. | 溶液中NH3的物质的量浓度为0.2mol•L-1 | |
| C. | NH3和NH3•H2O的物质的量浓度之和为0.2mol•L-1 | |
| D. | NH3、NH3•H2O和NH4+的物质的量之和为0.1mol |
9.现有一组物质:KCl、Na2SO4、NaCl、NH4Cl,某化学兴趣小组的同学进行了以下实验:
分别取少量上述溶液于4支试管中,然后分别加入Ba(OH)2溶液并加热,用湿润的红色石蕊试纸在试管口检验.上述操作不能鉴别出来的物质是KCl、NaCl.对于可以鉴别的物质,请填写表(可不填满):
分别取少量上述溶液于4支试管中,然后分别加入Ba(OH)2溶液并加热,用湿润的红色石蕊试纸在试管口检验.上述操作不能鉴别出来的物质是KCl、NaCl.对于可以鉴别的物质,请填写表(可不填满):
| 可以鉴别的物质 | 实验现象 | 有关反应的化学方程式 |
| . |
6.下列说法正确的是.
| A. | 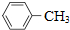 的一溴代物和 的一溴代物和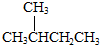 的一溴代物都有4种(不考虑立体异构) 的一溴代物都有4种(不考虑立体异构) | |
| B. | CH3CH=CHCH3分子中的四个碳原子在同一直线上 | |
| C. | 按系统命名法,化合物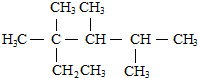 的名称是2,3,4-三甲基-2-乙基戊烷 的名称是2,3,4-三甲基-2-乙基戊烷 | |
| D. | 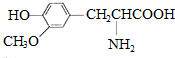 与 与 都是α-氨基酸且互为同系物 都是α-氨基酸且互为同系物 |
3.短周期主族元素X、Y、Z、W原子序数依次增大,X原子的最外层有6个电子,Y是迄今发现的非金属性最强的元素,在周期表中Z位于IA族,W与X属于同一主族.下列说法正确的是( )
| A. | 元素X、W的简单阴离子具有相同的电子层结构 | |
| B. | 由Y、Z两种元素组成的化合物是离子化合物 | |
| C. | W的简单气态氢化物的热稳定性比Y的强 | |
| D. | 原子半径:r(X)<r(Y)<r(Z)<r(W) |
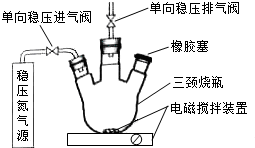 水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg•L-1.我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg•L-1.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.
水中溶氧量(DO)是衡量水体自净能力的一个指标,通常用每升水中溶解氧分子的质量表示,单位mg•L-1.我国《地表水环境质量标准》规定,生活饮用水源的DO不能低于5mg•L-1.某化学小组同学设计了下列装置(夹持装置略),测定某河水的DO.