题目内容
19.化学与生活密切相关.下列有关说法错误的是( )| A. | SiO2、MgO熔点高,可用于制作耐高温材料 | |
| B. | 天然气是可再生清洁能源,可用于工业制盐酸 | |
| C. | 硝酸铵属于氧化剂,严禁用可燃物(如纸袋)包装 | |
| D. | “一带一路”是“丝绸之路经济带”和“21世纪海上丝绸之路”的简称.丝绸的主要成分是蛋白质,属于高分子化合物 |
分析 A.耐高温材料应具有较高的熔点;
B.天然气属于化石燃料,是不可再生能源;
C.硝酸铵在有可被氧化的物质(还原剂)存在的条件下发生氧化还原反应,有爆炸的危险;
D.丝绸的成分为蛋白质,蛋白质是高分子化合物.
解答 解:A.SiO2、MgO熔点高,一般条件下不易熔融,所以可以用于制作耐高温仪器,故A正确;
B.天然气属于不可再生的清洁能源,故B错误;
C.硝酸铵属于氧化剂,应储存于阴凉、通风的库房,远离火种、热源,应与易(可)燃物、还原剂、酸类、活性金属粉末分开存放,故C正确;
D.丝绸的主要原料为蚕丝,蚕丝成分为蛋白质,蛋白质是高分子化合物,故D正确;
故选B.
点评 本题考查了化学知识在生活实际的应用,为高考常见题型,熟悉物质的组成、性质、用途等即可解答,题目有利于培养学生良好的科学素养,提高学习的积极性,难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案
相关题目
9.24mL 0.05mol•L -1的Na2SO3溶液,恰好跟20mL浓度为0.02mol•L -1的重铬酸钾(K2Cr2O7)溶液完全反应,则元素铬(Cr)在还原产物中的化合价是( )
| A. | +3 | B. | +2 | C. | +1 | D. | +6 |
10.薄荷醇有清凉作用,结构简式如图.下列有关薄荷醇的说法错误的是( )


| A. | 属于烃的衍生物 | B. | 烃基上的一氯取代物有9种 | ||
| C. | 与乙醇互为同系物 | D. | 能与乙酸发生酯化反应 |
7.下列实验中,为实现实验目的必须除杂,其中正确的是( )
| 实验 | 除杂试剂 | 实验目的 | |
| ① | CH3CH2Br与NaOH溶液共热 | HNO3溶液 | 用AgNO3溶液检验CH3CH2Br中的Br |
| ② | 淀粉与稀H2SO4水浴共热 | HNO3溶液 | 用银氨溶液检验水解产物的还原性 |
| ③ | C2H5OH与浓 H2SO4加热至170℃ | NaOH溶液 | 用KMnO4溶液证明该反应为消去反应 |
| ④ | 苯与液溴反应 | CCl4 | 用AgNO3溶液证明该反应为取代反应 |
| A. | ①②③④ | B. | 只有③④ | C. | 只有①②④ | D. | 只有①③④ |
14.实验室拟制备纯净的氯气并回收剩余药品,下列图示装置和原理能达到实验目的是( )
| A. |  制备Cl2 | B. | 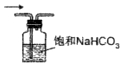 去除杂质 | C. |  干燥Cl2 | D. |  回收固体MnO2 |
4.以下事实不能用元素周期律解释的是( )
| A. | H2O在4000℃以上开始明显分解,H2S用酒精灯加热即可完全分解 | |
| B. | F2在暗处遇H2即爆炸,I2在暗处遇H2几乎不反应 | |
| C. | “NO2球”在冷水中颜色变浅,在热水中颜色加深 | |
| D. | 氯与钠形成离子键,氯与硅形成共价键 |
11.NA为阿伏加德罗常数的值.下列叙述错误的是( )
| A. | 1 mol 乙烯分子中含有的碳氢键数为4NA | |
| B. | 1 mol 甲烷完全燃烧转移的电子数为8NA | |
| C. | 1 L 0.1 mol•L-1的乙酸溶液中含H+的数量为0.1NA | |
| D. | 1 mol 的CO和N2混合气体中含有的质子数为14NA |
12. 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
 锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )
锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景.该电池通过一种复杂的铜腐蚀“现象”产生电力,其中放电过程为2Li+Cu2O+H2O═2Cu+2Li++2OH-,下列说法不正确的是( )| A. | 放电时,正极的电极反应式为Cu2O+H2O+2e-=2Cu+2OH- | |
| B. | 放电时,电子透过固体电解质向Li极移动 | |
| C. | 通空气时,铜被腐蚀,表面产生Cu2O | |
| D. | 整个反应过程中,氧化剂为O2 |
13.下列选用的仪器和药品能达到实验目的是( )
| A.准确量取一定体积的KMnO4 | B.验证Ba(OH)2•8H2O与NH4Cl晶体反应的吸放热 | C.制NH3的发生装置 | D.排空气法收集CO2 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |