题目内容
有机物A只含有C、H、O三种元素,常用作有机合成的中间体. 16.8g该有机物经燃烧生成44.0gCO2和14.4gH2O;质谱图表明其相对分子质量为84,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1.
(1)A的分子式为 .
(2)符合上述要求A的结构简式为 .
(1)A的分子式为
(2)符合上述要求A的结构简式为
考点:有关有机物分子式确定的计算
专题:
分析:(1)有机物A只含有C、H、O三种元素,其相对分子质量为84,16.8g有机物A的物质的量为:
=0.2mol,燃烧生成44.0g CO2的物质的量为:
1mol,生成14.4g H2O的物质的量为:
=0.8mol,故有机物A中C原子数目为:
=5,H原子数目为
=8,根据相对分子量计算出含有氧原子的数目,然后写出A的分子式;
(2)该有机物的不饱和度为:
=2,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,故分子中含有2个CH3、1个-OH连接在同一C原子上,据此写出有机物A的结构简式.
| 16.8g |
| 84g/mol |
| 44g |
| 44g/mol |
| 14.4g |
| 18g/mol |
| 1mol |
| 0.2mol |
| 0.8mol×2 |
| 0.2mol |
(2)该有机物的不饱和度为:
| 5×2+2-8 |
| 2 |
解答:
解:(1)有机物A只含有C、H、O三种元素,其相对分子质量为84,16.8g有机物A的物质的量为:
=0.2mol,燃烧生成44.0g CO2的物质的量为:
1mol,生成14.4g H2O的物质的量为:
=0.8mol,故有机物A中C原子数目为:
=5,H原子数目为
=8,故氧原子数目为:
=1,故A的分子式为:C5H8O,
故答案为:C5H8O;
(2)有机物A的不饱和度为:
=2,红外光谱分析表明A分子中含有O-H键和位于分子端的C≡C键,核磁共振氢谱有三个峰,峰面积为6:1:1,则该有机物分子中含有2个CH3、1个-OH连接在同一C原子上,所以A的结构简式为: ,
,
故答案为: .
.
| 16.8g |
| 84g/mol |
| 44g |
| 44g/mol |
| 14.4g |
| 18g/mol |
| 1mol |
| 0.2mol |
| 0.8mol×2 |
| 0.2mol |
| 84-12×5-8 |
| 16 |
故答案为:C5H8O;
(2)有机物A的不饱和度为:
| 5×2+2-8 |
| 2 |
 ,
,故答案为:
 .
.
点评:本题考查有机物分子式、结构简式的计算,题目难度中等,明确有机物结构与性质为解答本题的据此,注意掌握确定常见有机物分子式、结构简式的方法,试题有利于培养学生的分析、理解能力及化学计算能力.

练习册系列答案
相关题目
下列各组物质相互混合反应后,既有气体生成,最终又有沉淀生成的是( )
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2浓溶液和NH4Al(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2O2投入FeCl2溶液中.
①金属钠投入到FeCl3溶液中
②过量Ba(OH)2浓溶液和NH4Al(SO4)2溶液混合
③少量Ca(OH)2投入过量NaHCO3溶液中
④Na2O2投入FeCl2溶液中.
| A、只有①④ | B、只有③ |
| C、只有②③ | D、只有①②④ |
向NaBr、NaI、Na2SO3混合液中,通入-定量氯气后,将溶液蒸干并充分灼烧,得到固体剩余物质的组成不可能是( )
| A、NaCl Na2SO4 |
| B、NaCl NaBr Na2SO4 |
| C、NaCl NaBr NaI Na2SO4 |
| D、NaCl NaI Na2SO4 |
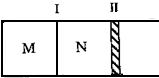 如图所示,隔板I固定不动,活塞II可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )
如图所示,隔板I固定不动,活塞II可自由移动.M、N两个容器中均发生如下反应:A(g)+3B(g)?2C(g);△H<0.若起始时,M、N容积相同.下列说法正确的是( )| A、起始时,分别向M、N两个容器中加入1molA、1molB,达平衡时,容器M、N中物质A的体积分数相同 |
| B、起始时,分别向M、N两个容器中加入1molA、3molB,达平衡时,容器M中物质A的转化率较大 |
| C、起始时,分别向M、N两个容器中加入2molC,容器N达到平衡所需的时间较短 |
| D、起始时,分别向M、N两个容器中加入1molA、3molB,达到平衡时,容器M中气体的密度较小 |
下列有机反应中,能够实现的是( )
A、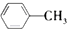 +Cl2 +Cl2
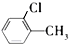 +HCl +HCl | |||
B、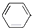 +CH2═CH-CH3 +CH2═CH-CH3
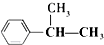 | |||
C、ClCH2CH2CH3+NaOH
| |||
D、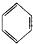 +2HONO2 +2HONO2
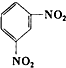 +2H2O +2H2O |
 用如图所示装置(夹持仪器已省略)进行实验,E为分液漏斗活塞.将液体A逐滴加入到固体B 中,请回答下列问题:
用如图所示装置(夹持仪器已省略)进行实验,E为分液漏斗活塞.将液体A逐滴加入到固体B 中,请回答下列问题: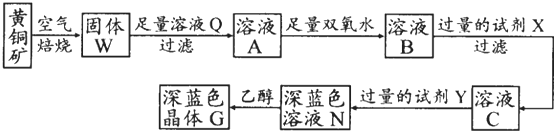
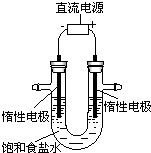 电解饱和食盐水的装置如图所示,若收集的H2为2 L,则同样条件下收集Cl2小于2 L,原因是
电解饱和食盐水的装置如图所示,若收集的H2为2 L,则同样条件下收集Cl2小于2 L,原因是