题目内容
探究外界条件对化学反应速率的影响常用到该反应已知:Na2S2O3+H2SO4→Na2SO4+S↓+SO2+H2O
针对上述反应涉及到的元素或物质及性质回答有关问题:
(1)硫元素的化合价由高到低顺序为: 涉及元素的简单离子半径由小到大顺序为: .
针对上述反应涉及到的元素或物质及性质回答有关问题:
(1)硫元素的化合价由高到低顺序为:
考点:常见元素的化合价,微粒半径大小的比较
专题:
分析:根据化合物中元素化合价的代数和为零计算;离子的电子层数越多,半径越大,电子层数相同时,原子序数越大,半径越小,据此分析.
解答:
解:化合物中元素化合价的代数和为零,则Na2S2O3中硫元素的化合价为+2价,H2SO4中硫元素的化合价为Na2SO4+6价,S是单质硫元素的化合价为0价,SO2中硫元素的化合价为+4价,则硫元素的化合价由高到低顺序为:+6、+4、+2、0;
离子的电子层数越多,半径越大,电子层数相同时,原子序数越大,半径越小,则元素的简单离子半径由小到大顺序为:H+<Na+<O2-<S2-;
故答案为:+6、+4、+2、0; H+<Na+<O2-<S2-.
离子的电子层数越多,半径越大,电子层数相同时,原子序数越大,半径越小,则元素的简单离子半径由小到大顺序为:H+<Na+<O2-<S2-;
故答案为:+6、+4、+2、0; H+<Na+<O2-<S2-.
点评:本题考查了元素化合价的计算和离子半径大小比较,题目难度不大,注意把握离子半径大小的比较方法.

练习册系列答案
相关题目
用无机矿物资源生产部分材料,其产品流程示意图如下:下列有关说法不正确的是( )
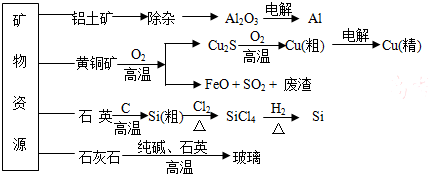

| A、制取玻璃的同时产生CO2气体,制取粗硅时生成的气体产物为CO |
| B、生产高纯硅、铝、铜及玻璃的过程中都涉及氧化还原反应 |
| C、粗硅制高纯硅时,提纯四氯化硅可用多次蒸馏的方法 |
| D、黄铜矿冶炼铜时产生的SO2可用于生产硫酸,FeO可用作冶炼铁的原料 |
少量SO2通入“84消毒液”中,其离子反应方程式最合理的是( )
| A、H2SO3+ClO-→H++SO42-+Cl- |
| B、SO2+ClO-+H2O→H++SO42-+Cl- |
| C、SO2+ClO-+H2O→SO32-+HClO |
| D、SO2+ClO-+2OH-→SO42-+Cl-+H2O |
136C可以用于含碳化合物的结构分析,下列有关136C 的说法不正确的是( )
| A、核内有7个中子 |
| B、核内有6个质子 |
| C、质量数为13 |
| D、与石墨互为同位素 |
将15.6g Na2O2和5.4g Al同时放入一定量的水中,充分反应后得到200mL溶液,再向该溶液中缓慢通入标准状况下的HCl气体6.72L,若反应过程中溶液的体积保持不变,则下列说法正确的是( )
| A、最终溶液:c(Na+)=1.5mol/L |
| B、标准状况下,反应过程中得到6.72 L气体 |
| C、最终溶液:c(Na+)=c(Cl-) |
| D、最终得到7.8 g沉淀 |