题目内容
在含有Fe3+、Fe2+、Al3+、NH 的稀溶液中,加入足量的Na2O2固体并微热,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有明显变化的是
的稀溶液中,加入足量的Na2O2固体并微热,充分反应后,再加入过量的稀盐酸,完全反应后,离子数目没有明显变化的是
A.Fe3+ B.Fe2+ C.NH D.Al3+
D.Al3+
D
【解析】
试题分析:Na2O2固体放入水中,会发生反应:2Na2O2+2H2O=4NaOH+ O2↑,产生的氧气有氧化性,会把Fe2+氧化为Fe3+,产生的NaOH与 Al3+反应形成NaAlO2,与Fe3+形成Fe(OH)3沉淀;与NH反应在加入时会产生氨气逸出,充分反应后,再加入过量的稀盐酸,Fe(OH)3变为Fe3+;NaAlO2变为Al3+。所以完全反应后,离子数目没有明显变化的是Al3+,选项是D。
考点:考查元素集化合物的性质及转化的知识。

 发散思维新课堂系列答案
发散思维新课堂系列答案(10分)氧化还原反应中实际上包含氧化和还原两个过程。下面是一个还原过程的反应式:
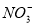 +4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
+4H++3e-=NO+2H2O。KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生。
(1)写出并配平该氧化还原反应的方程式:______________。
(2)反应中硝酸体现了________、_________的性质。
(3)反应中若产生0.2 mol气体,则转移电子的物质的量是___________mol。
(4)若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是___________。
X 、Y、Z、W是中学化学常见的四种物质,他们之间具有如图所示转化关系,则下列组合不可能的是
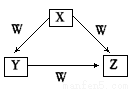
| X | Y | Z | W |
A | C | CO | CO2 | O2 |
B | Na | Na2O | Na2O2 | O2 |
C | AlCl3 | Al(OH)3 | NaAl(OH)4 | NaOH |
D | Fe | FeCl2 | FeCl3 | Cl2 |
化学与社会、生活密切相关。对下列现象或事实的解释正确的是
选项 | 现象或事实 | 解 释 |
A | 用浸泡酸性高锰酸钾溶液的硅土延长果实的成熟 | 利用乙烯可以发生加成反应
|
B | 施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用 | K2CO3与NH4Cl反应生成氨气会降低肥效 |
C | SO2能使品红溶液褪色 | SO2具有还原性 |
D | FeCl3溶液可用于铜质印刷线路板制作 | FeCl3能从含有Cu2+的溶液中置换出铜 |