题目内容
12.由乙烯可生产多种化工原料,根据如图所示的转化关系回答问题:
(1)写出下列物质的结构简式:ACH3CH2OH;BCH3CHO;CCH3COOCH2CH3.
(2)反应①~⑥中,属于取代反应的是④⑥(填序号).
(3)反应②的化学方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O.
(4)反应⑤的化学方程式为CH3COOH+H2O2→CH3COOOH+H2O.
(5)重要化工原料氯乙酸(CH2Cl-COOH)与水反应可得到羟基乙酸(HOCH2-COOH),羟基乙酸与反应⑤的产物过氧乙酸互为同分异构体(选填“同系物”、“同分异构体”、“同素异形体”或“同位素”).
分析 乙烯属于不饱和烃,分子中含有碳碳双键官能团.所以可发生加成反应,和水加成生成物A是CH3CH2OH,乙醇与氧气发生氧化得B为CH3CHO,乙醛被氧化生成乙酸,乙酸和乙醇发生反应生成C为CH3COOCH2CH3,结合对应物质的性质以及题目要求解答该题.
解答 解:乙烯属于不饱和烃,分子中含有碳碳双键官能团.所以可发生加成反应,和水加成生成物A是CH3CH2OH,乙醇与氧气发生氧化得B为CH3CHO,乙醛被氧化生成乙酸,乙酸和乙醇发生反应生成C为CH3COOCH2CH3,
(1)由以上分析可知A为CH3CH2OH,B为CH3CHO,C为CH3COOCH2CH3,故答案为:CH3CH2OH;CH3CHO;CH3COOCH2CH3;
(2)由转化关系可知①~⑥的反应类型依次为:加成、氧化、氧化、取代、氧化、取代反应,则属于取代反应的为④⑥,故答案为:④⑥;
(3)乙醇与氧化铜发生氧化反应生成乙醛,方程式为CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O,故答案为:CH3CH2OH+CuO$\stackrel{△}{→}$CH3CHO+Cu+H2O;
(4)反应⑤的化学方程式为CH3COOH+H2O2→CH3COOOH+H2O,故答案为:CH3COOH+H2O2→CH3COOOH+H2O;
(5)羟基乙酸与反应⑤的产物过氧乙酸分子式相同,但结构不同,互为同分异构体,故答案为:同分异构体.
点评 本题考查有机物推断,为高频考点,以A为突破口结合反应条件进行推断,熟悉常见有机物结构简式、官能团及其性质关系,题目难度不大.

练习册系列答案
相关题目
2.白钨矿的主要成分是钨酸钙(CaWO4),其中钨的化合价为( )
| A. | +3 | B. | +4 | C. | +6 | D. | +7 |
20.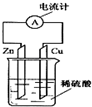 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
 如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )
如图所示,把锌片和铜片用导线相连后插入稀硫酸溶液中构成原电池.下列叙述正确的是( )| A. | 该装置将电能转变为化学能 | B. | 电流从锌片经导线流向铜片 | ||
| C. | 一段时间后,铜片质量减轻 | D. | 锌片上发生氧化反应 |
7.下列实验能获得成功的是( )
| A. | 制备溴苯时,将苯与溴水混合,剧烈振荡 | |
| B. | 除去甲烷中混有的二氧化碳时,依次通过烧碱溶液和浓硫酸 | |
| C. | 在酸性高锰酸钾溶液中滴加几滴苯,用力振荡,紫红色褪去 | |
| D. | 在苯中铜氢气制备环己烷 |
17.下列说法错误的是( )
| A. | 食物放在冰箱中会减慢食物变质的速率 | |
| B. | 钾的金属性强,所以钾与水的反应比钠的反应剧烈 | |
| C. | 2mol SO2与1mol O2混合反应后一定能生成2 mol SO3 | |
| D. | 面粉厂严禁烟火的原因是面粉粉尘表面积大,与空气接触遇明火极易发生爆炸 |
4.用NA表示阿伏加德罗常数的值,下列判断正确的是( )
| A. | 44gN2O含有的氮原子数目为NA | |
| B. | 常温常压下,22.4 L N2含有的分子数目为NA | |
| C. | 1 mol Mg变为Mg2+时失去的电子数目为2NA | |
| D. | lmol•L-1K2CO3,溶液中含有的钾离子数目为NA |
1.纯水中存在如下平衡:H2O?H++OH-△H>0,当改变条件时,填写表中各项内容.
| 改变条件 | 平衡移动方向 | pH | 水电离出的c(H+) | KW |
| 升温 | ||||
| 通入HCl气体 | ||||
| 加入NaOH固体 | ||||
| 加入NH4Cl固体 | ||||
| 加入金属钠 |
1.下列说法正确的是( )
| A. | 10 g氖气所含原子数为6.02×1023 | |
| B. | 25℃时,pH=6的水溶液中c(H+)>c(OH-) | |
| C. | 实验室制氢气时加入少量CuSO4可加快反应速率是利用了盐类的水解 | |
| D. | 把16.0 g无水硫酸铜粉末放在足量饱和硫酸铜溶液中会析出25.0 g晶体 |