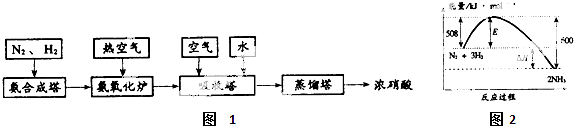
��Ŀ����
��֪��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol������Ŀǰ�ձ�ʹ�õ��˹��̵��ķ�������ش��������⣺
��1��450��ʱ����һ��2L���ܱ������г���2.6mol H2��1mol N2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±���ʾ��
�ٴ������¸÷�Ӧ�Ļ�ѧƽ�ⳣ��K= ����Ӧ�ﵽƽ�������ƽ����ϵ�м���H2��N2��NH3��2mol����ʱ�÷�Ӧ��v��N2���� v��N2��������д����������=������=����
�����ı�ijһ����������ƽ��ʱn��H2��=1.60mol������˵����ȷ���� ��
A��ƽ��һ�������ƶ� B���������������м�����һ������H2����
C�������ǽ������������¶� D����������С�����������
��2��450��ʱ������һ�ܱ������н��������ϳɰ��ķ�Ӧ�������ʵ���ʼŨ�Ⱥ�ƽ��Ũ�����±���ʾ��
��ش�
��a��ȡֵ��Χ�ǣ� ��
��������ѧ����ʽ��ʾ������֮��Ĺ�ϵ����I��a��b�Ĺ�ϵ�� ������a��b��c�Ĺ�ϵ�� ��
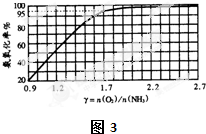
�۷�Ӧ�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ������t2�pt7ʱ������Ӧ��ʵ�������ı�ֱ��ǣ�t2 ��t7 ��

��1��450��ʱ����һ��2L���ܱ������г���2.6mol H2��1mol N2����Ӧ�����ж�NH3��Ũ�Ƚ��м�⣬�õ����������±���ʾ��
| ʱ��/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c��NH3��/mol?L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
�����ı�ijһ����������ƽ��ʱn��H2��=1.60mol������˵����ȷ����
A��ƽ��һ�������ƶ� B���������������м�����һ������H2����
C�������ǽ������������¶� D����������С�����������
��2��450��ʱ������һ�ܱ������н��������ϳɰ��ķ�Ӧ�������ʵ���ʼŨ�Ⱥ�ƽ��Ũ�����±���ʾ��
| N2 | H2 | NH3 | |
| ��ʼŨ�ȣ�mol/L�� | 0.2 | 0.3 | 0.2 |
| ƽ��Ũ�ȣ�mol/L�� | a | b | c |
��a��ȡֵ��Χ�ǣ�
��������ѧ����ʽ��ʾ������֮��Ĺ�ϵ����I��a��b�Ĺ�ϵ��
�۷�Ӧ�ﵽƽ��ı�ijһ�����������Ӧ������ʱ��Ĺ�ϵ��ͼ��ʾ������t2�pt7ʱ������Ӧ��ʵ�������ı�ֱ��ǣ�t2

���㣺��ѧƽ��ļ���,��ѧ��Ӧ�����뻯ѧƽ��ͼ����ۺ�Ӧ��
ר�⣺��ѧƽ��ר��
��������1���ٸ��ݻ�ѧƽ������ʽ���㣬ȷ����Ӧ�ﵽƽ������ʵı仯���ͷ�Ӧ�ﵽ��ѧƽ��ʱ�����ʵ�Ũ�ȣ������������ʺ�ƽ�ⳣ��������ƽ��״̬���ж������жϣ�ֻҪ��������Ӧ���ʵ����淴Ӧ���ʣ������жϣ�
������������������غ�ƽ���ƶ����з����жϣ�
��2�����ݼ�ֵת�����ҵ������ʵ�Ũ�ȷ�Χ���з����жϣ�����ƽ�ⳣ���������abc�Ĺ�ϵ��
��3������ͼ��ͷ�Ӧ���������ƽ���ƶ�ԭ�������жϷ��ϸı��������
������������������غ�ƽ���ƶ����з����жϣ�
��2�����ݼ�ֵת�����ҵ������ʵ�Ũ�ȷ�Χ���з����жϣ�����ƽ�ⳣ���������abc�Ĺ�ϵ��
��3������ͼ��ͷ�Ӧ���������ƽ���ƶ�ԭ�������жϷ��ϸı��������
���
�⣺��1���ٸ���������ʽ���㣬�ӱ��з�����֪��20minʱ��Ӧ�Ѵ�ƽ�⣬C��NH3��=0.20mol/L
���ݷ�Ӧ N2 +3H2
2NH3
��ʼŨ�ȣ�mol/L����0.5 1.3 0
�仯Ũ�ȣ�mol/L����0.1 0.3 0.2
ƽ��Ũ�ȣ�mol/L����0.4 1.0 0.2
K=
=
=0.1��L/mol��2
��Ӧ�ﵽƽ�������ƽ����ϵ�м���H2��N2��NH3��2mol����ʱ������������������Ũ�ȷֱ�Ϊ��
0.4+1=1.4mol/L��1.0+1=2mol/L��0.2+1=1.2mol/L������Ũ����
Q=
=
=0.13��L/mol��2
Q��K��ƽ����������У�v��N2������v��N2����
�ʴ�Ϊ��0.1������
����ԭƽ��״̬�������ʵ���Ϊ2mol���ı�ijһ����������ƽ��ʱn��H2��=1.60mol��˵���������٣������Ǹı�����ƽ��������У���������������
A��ƽ�ⲻһ��������У����������������Է��ϣ���A����
B���������������м�����һ������H2���壬ʹ����������B����
C���÷�Ӧ�Ƿ��ȷ�Ӧ���������������¶ȣ�ƽ��������Ӧ������У������������٣���C��ȷ��
D����С������������൱������ѹǿ��ƽ�������������С�ķ�����У��÷�Ӧ����������������ٵķ�Ӧ��������С�����ƽ��������У������������٣��������С������Ũ�������ƽ���ƶ����������ļ��ٳ̶�С�����տ�������������С����D��ȷ��
�ʴ�Ϊ��CD��
��2������ƽ�����ķ�����ʽ����
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.2 0.3 0.2
�仯����mol/L��
ƽ������mol/L�� a b c
��Ӧ��������� 0.1 0 0.4
��Ӧ��������� 0.3 0.6 0
����ƽ��ʱŨ�ȵ�ȡֵ��Χ��0.1��a��0.3 0��b��0.6 0��c��0.4
��a��ȡֵ��Χ��0.1��a��0.3��
�ʴ�Ϊ��0.1��a��0.3��
�����ü�ֵת�����м���
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.2 0.3 0.2
ƽ������mol/L�� a b c
��ֵת�� a+0.5c b+1.5c 0
a+0.5c=0.2
b+1.5c=0.3��
�����ã�a��b�Ĺ�ϵΪ 3a=b+0.3��a��b��c�Ĺ�ϵ���¶ȱ仯��ƽ�ⳣ�����䣬K=0.1������ƽ�ⳣ������ʽ����õ���
=0.1
�ʴ�Ϊ��3a=b+0.3��
=0.1��
��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol����Ӧ�����������С�ķ��ȷ�Ӧ��t2ʱ�̷�Ӧ������У��淴Ӧ����С��ԭƽ������Ȼ������˵���ı�����������ӷ�Ӧ��Ũ�ȣ�ͬʱ��С������Ũ�ȣ�t7ʱ�����淴Ӧ���ʶ���С���ҷ�Ӧ������Ӧ������У�˵���ǽ����¶ȣ�ƽ��������У�
�ʴ�Ϊ�����ӷ�Ӧ��Ũ�ȣ�ͬʱ��С������Ũ�ȣ������¶ȣ�
���ݷ�Ӧ N2 +3H2
| ||
| �� |
��ʼŨ�ȣ�mol/L����0.5 1.3 0
�仯Ũ�ȣ�mol/L����0.1 0.3 0.2
ƽ��Ũ�ȣ�mol/L����0.4 1.0 0.2
K=
| c2(NH3) |
| c(N2)c3(H2) |
| 0��22 |
| 0.4��1��03 |
��Ӧ�ﵽƽ�������ƽ����ϵ�м���H2��N2��NH3��2mol����ʱ������������������Ũ�ȷֱ�Ϊ��
0.4+1=1.4mol/L��1.0+1=2mol/L��0.2+1=1.2mol/L������Ũ����
Q=
| c2(NH3) |
| c(N2)c3(H2) |
| 1��22 |
| 1.4��23 |
Q��K��ƽ����������У�v��N2������v��N2����
�ʴ�Ϊ��0.1������
����ԭƽ��״̬�������ʵ���Ϊ2mol���ı�ijһ����������ƽ��ʱn��H2��=1.60mol��˵���������٣������Ǹı�����ƽ��������У���������������
A��ƽ�ⲻһ��������У����������������Է��ϣ���A����
B���������������м�����һ������H2���壬ʹ����������B����
C���÷�Ӧ�Ƿ��ȷ�Ӧ���������������¶ȣ�ƽ��������Ӧ������У������������٣���C��ȷ��
D����С������������൱������ѹǿ��ƽ�������������С�ķ�����У��÷�Ӧ����������������ٵķ�Ӧ��������С�����ƽ��������У������������٣��������С������Ũ�������ƽ���ƶ����������ļ��ٳ̶�С�����տ�������������С����D��ȷ��
�ʴ�Ϊ��CD��
��2������ƽ�����ķ�����ʽ����
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.2 0.3 0.2
�仯����mol/L��
ƽ������mol/L�� a b c
��Ӧ��������� 0.1 0 0.4
��Ӧ��������� 0.3 0.6 0
����ƽ��ʱŨ�ȵ�ȡֵ��Χ��0.1��a��0.3 0��b��0.6 0��c��0.4
��a��ȡֵ��Χ��0.1��a��0.3��
�ʴ�Ϊ��0.1��a��0.3��
�����ü�ֵת�����м���
N2��g��+3H2��g��?2NH3��g��
��ʼ����mol/L�� 0.2 0.3 0.2
ƽ������mol/L�� a b c
��ֵת�� a+0.5c b+1.5c 0
a+0.5c=0.2
b+1.5c=0.3��
�����ã�a��b�Ĺ�ϵΪ 3a=b+0.3��a��b��c�Ĺ�ϵ���¶ȱ仯��ƽ�ⳣ�����䣬K=0.1������ƽ�ⳣ������ʽ����õ���
| c2 |
| a��b3 |
�ʴ�Ϊ��3a=b+0.3��
| c2 |
| a��b3 |
��N2��g��+3H2��g��?2NH3��g����H=-92.4kJ/mol����Ӧ�����������С�ķ��ȷ�Ӧ��t2ʱ�̷�Ӧ������У��淴Ӧ����С��ԭƽ������Ȼ������˵���ı�����������ӷ�Ӧ��Ũ�ȣ�ͬʱ��С������Ũ�ȣ�t7ʱ�����淴Ӧ���ʶ���С���ҷ�Ӧ������Ӧ������У�˵���ǽ����¶ȣ�ƽ��������У�
�ʴ�Ϊ�����ӷ�Ӧ��Ũ�ȣ�ͬʱ��С������Ũ�ȣ������¶ȣ�
���������⿼���˻�ѧƽ��ļ��㣬���ʡ�ƽ�ⳣ���ļ��㣬ƽ��״̬���ж����ݺͷ�����Ӱ��ƽ������ط�������˹���ɵ�Ӧ�ã��ؼ��Ǽ�ֵ���ڻ�ѧƽ���е�Ӧ�ã���Ŀ�ۺ���ǿ�����ѣ�

��ϰ��ϵ�д�
 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
�����Ŀ
����������ȷ���ǣ�������
| A����AlCl3��Һ�еμӰ�ˮ��������ɫ�������ټ�������NaHSO4��Һ��������ʧ |
| B����ϡ�����м���ͭ�ۣ�ͭ�۲��ܽ⣻�ټ���Cu��NO3��2���壬ͭ���Բ��ܽ� |
| C����CO2ͨ��BaCl2��Һ�������ͣ�������������ͨ��SO2���������� |
| D����п��ϡ���ᷴӦ�������������ʽ������ټ�������CuSO4���壬���ʼӿ� |
��120�棬101Kpa�£����и����������Ժ��ֱ�����ϣ������������е�ȼ���ָ���ԭ״�����û�б仯���ǣ�������
| A��CH4 C2H8 |
| B��C2H4 C2H2 |
| C��C2H2 C2H6 |
| D��CH4 C2H4 |

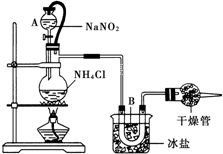 ʵ���ҳ��ñ���NaNO2��NH4Cl��Һ��Ӧ��ȡ������������ͼ����ӦʽΪ��NaNO2+NH4Cl�TNaCl+N2��+2H2O����Ӧ���ȣ��Իش�
ʵ���ҳ��ñ���NaNO2��NH4Cl��Һ��Ӧ��ȡ������������ͼ����ӦʽΪ��NaNO2+NH4Cl�TNaCl+N2��+2H2O����Ӧ���ȣ��Իش�