题目内容
某盐的混合物中含有0.2 mol/L Na+、0.4 mol/L Mg2+、0.4 mol/L Clˉ,则SO42ˉ为
A.0.1 mol/L B.0.2 mol/L
C.0.3 mol/L D.0.4 mol/L
C
【解析】
试题分析:盐的混合物中含有0.2mol/L Na+、0.4mol/L Mg2+、0.4mol/L Clˉ,根据溶液呈电中性,则有2c(Mg2+)+c(Na+)=c(Cl-)+2c(SO42-),则2c(SO42-)=2c(Mg2+)+c(Na+)-c(Cl-)=2×0.4mol/L+0.2mol/L-0.4mol/L=0.6mol/L,所以c(SO42-)=0.3mol/L。
考点:考查物质的量浓度的相关计算。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
仅用下表提供的玻璃仪器(非玻璃仪器任选)或实验装置(图1、图2)就能实现相应实验目的是
选项 | A | B | C | D |
实验项目 | 除去KCl中少 的 MnO2 | 用10mol/L的盐酸配制100mL0.1mol/L的盐酸 | 用氯化钠溶液制备氯化钠晶体 | 除去CO2气体中的HCl |
实验仪器 或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |
图1 |
图2 |


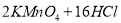 (浓)====
(浓)==== 

 溶液吸收氯气防止污染。写出该反应的离子方程式 。
溶液吸收氯气防止污染。写出该反应的离子方程式 。


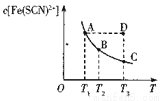
 Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是
Fe(SCN)2+(aq) 已知某一条件下,反应达到平衡时,Fe(SCN)2+的物质的量浓度与温度的关系如图所示,下列说法正确的是