题目内容
9.4.8g铜100mL的稀硝酸中,铜完全反应,(假设反应后溶液的体积不变).计算(1)生产气体的体积(标准状况下).
(2)生产硝酸铜的物质的量浓度.
分析 (1)根据n=$\frac{m}{M}$计算4.8g铜的物质的量,再根据3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O计算生成的NO的物质的量,根据V=nVm计算生成NO的体积;
(2)根据铜原子守恒可知n[Cu(NO3)2]=n(Cu),再根据c=$\frac{n}{V}$计算.
解答 解:(1)4.8g铜的物质的量=$\frac{4.8g}{64g/mol}$=0.075mol,则:
3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O
3 2
0.075mol n(NO)
故n(NO)=$\frac{2×0.075mol}{3}$=0.05mol,所以V(NO)=0.05mol×22.4L/mol=1.12L,
答:生成NO的体积为1.12L(标准状况下).
(2)n[Cu(NO3)2]=n(Cu)=0.075mol,c[Cu(NO3)2]=$\frac{0.075mol}{0.1L}$=0.75 mol/L,
答:生产硝酸铜的物质的量浓度为0.75 mol/L.
点评 本题考查根据方程式的计算、硝酸的性质等,比较基础,旨在考查学生对基础知识的理解掌握

练习册系列答案
相关题目
20.按图甲进行实验,若乙中横坐标x表示流入电极的电子的物质的量,下列叙述不正确的是( )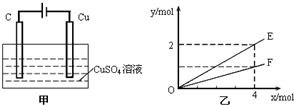

| A. | E表示生成铜的物质的量 | B. | E表示生成硫酸的物质的量 | ||
| C. | F表示反应消耗水的物质的量 | D. | E表示反应生成氧气的物质的量 |
17.某反应过程能量变化如图所示,下列说法正确的是( )


| A. | 改变催化剂,可改变该反应的活化能 | |
| B. | 该反应为放热反应,热效应等于E 1-E 2 | |
| C. | 反应过程 a 有催化剂参与 | |
| D. | 有催化剂条件下,反应的活化能等于 E 1+E 2 |
1.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol•L-1MgCl2溶液中含有的Mg2+数目一定小于0.1NA | |
| B. | 标准状况下,11.2 L CCl4中含有的分子数目为0.5NA | |
| C. | 4.6g由NO2和N2O4组成的混合物中含有氧原子的数目为0.2 NA | |
| D. | 1 mol CH${\;}_{5}^{+}$中含有的电子数目为11NA |
18.下列关于电解质的说法正确的是( )
| A. | 铜能导电但属于非电解质 | |
| B. | 氯化氢气体不能导电,所以氯化氢是非电解质 | |
| C. | 电解质不一定能导电 | |
| D. | SO2溶于水形成的溶液能导电,所以SO2是电解质 |
19.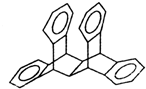 科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
( )
 科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是
科罗拉多大学的克利斯托(S.Cristol)等人合成了一种有机分子,这种分子让他想起罗马的两面神Janus--罗马的守门神,克利斯托的同事迈金泰(Macintyre)就建议将该分子叫做Janusene.该有机物的结构简式如图所示,下列说法正确的是( )
| A. | 该有机物的一氯代物只有4种(不包括立体异构) | |
| B. | 该有机物完全燃烧生成CO2和H2O的物质的量之比为15:11 | |
| C. | 该有机物属于苯的同系物 | |
| D. | 该有机物只能发生取代反应而不能发生加成反应 |