题目内容
14.下列变化过程中,需吸收能量的是( )| A. | H+H→H2 | B. | I2→I+I | C. | 木炭燃烧 | D. | 铝与稀盐酸反应 |
分析 常见的放热反应有:所有的物质燃烧、所有金属与酸、所有中和反应;绝大多数化合反应、置换反应;少数分解、复分解反应.
常见的吸热反应有:个别的化合反应(如C和CO2),绝大数分解反应、少数置换以及某些复分解反应(如铵盐和强碱).
物质在溶解时经常伴随有吸热或放热现象,氢氧化钠固体、浓硫酸溶于放出大量的热,温度升高;硝酸铵固体溶于水吸热,温度降低.
断裂化学键吸热,形成新的化学键放热.
解答 解:A.H+H→H2为氢原子与氢原子共用电子对,形成新的化学键H-H键放热,故A错误;
B.I2→I+I为碘原子、碘原子间共用电子对断裂,断裂化学键吸热,故B正确;
C.木炭燃烧,放出热量,属于典型的放热反应,故C错误;
D.所有金属与酸反应为放热反应,铝与稀盐酸反应属于放热反应,故D错误;
故选B.
点评 本题考查化学中吸热或放热问题,熟记吸热或放热的判断规律是正确解答此类题的关键,题目难度不大.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
4.下列叙述错误的是( )
| A. | 过程的自发性只能用于判断过程的方向性,不能确定过程是否一定会发生和过程发生的速率 | |
| B. | 空气污染日报中的空气污染指数的主要项日有可吸入颗粒物、二氧化硫、二氧化氮 | |
| C. | 金属冶炼过程主要是利用金属矿物中的金属离子失去电子变成金属单质所发生的氧化还原反应 | |
| D. | 糖类和油脂是重要的基本营养物质,并且是人体所需能量的重要来源 |
5.CuBr是一种白色晶体,见光或潮湿时受热易分解,在空气中逐渐变为浅绿色.实验室制备CuBr的反应原理为SO2+2CuSO4+2NaBr+2H2O═2CuBr↓+2H2SO4+Na2SO4,用下列装置进行实验,不能达到实验目的是( )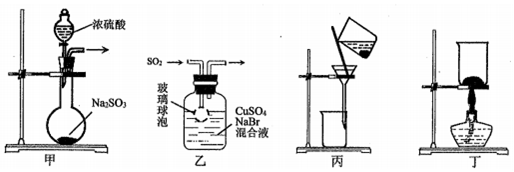

| A. | 用装置甲制取SO2 | B. | 用装置乙制取CuBr | ||
| C. | 用装置丙避光将CuBr与母液分离 | D. | 用装置丁干燥CuBr |
2.某固定体积的密闭容器中,加入一定量的A达化学平衡:aA(g)?bB(g)+cC(g),在温度不变的条件下,再充入一定量的A,重新达到平衡时,下列判断中正确的是( )
| A. | 若a=b+c时,B的物质的量分数变大 | B. | 若a=b+c时,B的体积分数不变 | ||
| C. | 若a>b+c时,A的转化率变小 | D. | 若a<b+c时,A的转化率变大 |
9.下列物质的类别与所含官能团都正确的是( )
| A. | 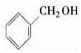 酚类-OH 酚类-OH | B. | CH3COCH3 醚类 C-O-C | ||
| C. | 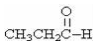 醛类-CHO 醛类-CHO | D. | 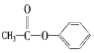 酮类 C═O 酮类 C═O |
19.下列说法正确的是( )
| A. | SO2与SO3互为同分异构体 | |
| B. | 氢气是理想的绿色能源 | |
| C. | 单质中不存在化学键 | |
| D. | 电解饱和氯化钠溶液可能得到金属钠 |
6.下列说法正确的是( )
| A. | 在合成塔中加入3molH2与1molN2反应即可得到2molNH3 | |
| B. | 工业上合成SO3时可加入过量空气以提高SO2的转化率 | |
| C. | 利用Al、Mg、NaOH溶液、导线及电流计等可证明Al的金属活动性大于Mg的 | |
| D. | 冰箱保存的食品不易变质,与化学反应速率无关 |
3.关于配合物[Cu(H2O)4]SO4,下列说法错误的是( )
| A. | 此配合物,中心离子的配位数为4 | |
| B. | H2O为配体,配位原子是氧原子 | |
| C. | 此配合物中,Cu2+提供孤对电子 | |
| D. | 向此配合物溶液中加入BaCl2溶液,出现白色沉淀 |
4.下列叙述错误的是( )
| A. | 常温下,向0.1mol/LNH4HSO4溶液中滴加NaOH溶液至中性C(Na+)>c(SO42-)>c(NH4+)>c(OH-)=C(H+) | |
| B. | 向饱和NaClO溶液中滴加少量饱和FeSO4溶液,反应的离子方程式为2Fe2++ClO-+5H2O═2Fe(OH)3↓+Cl-+4H+ | |
| C. | 0.2mol•L-1CH3COOH溶液与0.1mol•L-1 NaOH溶液等体积混合2c(H+)-2c(OH-)=c(CH2COO-)-c(CH2COOH) | |
| D. | 常温下cmol/L、电离常数为Ka的酸HA溶液中,由水电离的浓度为c(H+)水=$\frac{1{0}^{-14}}{\sqrt{Ka•c}}$mol•L-1 |