题目内容
3.NCl3的电子式为 ,则NCl3与H2O反应时.最初的生成物一定有( )
,则NCl3与H2O反应时.最初的生成物一定有( )| A. | NH3 | B. | HNO2 | C. | HClO | D. | NH4Cl |
分析 由于N是多电子原子,有一对孤对电子,所以NCl3与H2O反应时,水提供一个氢给中心氮原子后,剩余的OH跟Cl结合形成次氯酸,据此解答.
解答 解:由于N是多电子原子,有一对孤对电子,所以NCl3与H2O反应时,水提供一个氢给中心氮原子后,剩余的OH跟Cl结合形成次氯酸,所以NCl3与H2O反应时.最初的生成物一定有NH3、HClO,
故选:AC.
点评 本题考查了化学反应机理,明确氮原子结构特点是解题关键,题目难度中等.

练习册系列答案
 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
13.下列除杂质选用试剂和主要操作都正确的是( )
| 物质 | 杂质 | 试剂 | 主要操作 | |
| A | SiO2 | Fe2O3 | 盐酸 | 过滤 |
| B | NaHCO3 | NH4Cl | - | 加热 |
| C | Fe | Al | 氢氧化钠 | 洗气 |
| D | 乙烷 | 乙烯 | 溴水 | 蒸馏 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
14.《本草纲目》卷七记载“石碱条”:“彼人采蒿蓼之属,晒干烧灰,以水淋汁,久则凝淀如石,浣衣发面,亦去垢发面”.此处“石碱条”是指( )
| A. | K2CO3 | B. | Na2SO4 | C. | Ca(OH)2 | D. | Na2CO3 |
11.有四组同一族元素所形成的不同物质,在101kPa时测定它们的沸点(℃)如表所示:
下列各项判断不正确的是( )
| 第一组 | A-268.8 | B-249.5 | C-185.8 | D-151.7 |
| 第二组 | F2-187.0 | Cl2-33.6 | Br2 58.7 | I2 184.0 |
| 第三组 | HF 19.4 | HCl-84.0 | HBr-67.0 | HI-35.3 |
| 第四组 | H2O 100.0 | H2S-60.2 | H2Se-42.0 | H2Te-1.8 |
| A. | 第四组物质中H2O的沸点最高,是因为H2O分子之间存在氢键 | |
| B. | 第三组与第四组相比较,化合物的稳定性顺序为:HBr>H2Se | |
| C. | 第二组物质,单质的氧化性:F2>Cl2>Br2>I2 | |
| D. | 第一组物质是分子晶体,一定含有共价键 |
18.下列说法正确的是( )
| A. | T℃时,测得某NaNO2溶液的pH=8,则溶液中c(Na+)_c(NO2-)=9.9×10-7mol•L-1 | |||||||||
| B. | 已知H3PO2(次磷酸)是一种一元中强酸,则其与NaOH所形成的酸式盐NaH2PO2溶液中存在下列离子浓度大小关系c(Na+)>c(H2PO2-)c(OH-)>c(H+) | |||||||||
| C. | 一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如表数据:
| |||||||||
| D. |  已知,某温度时Ag2SO4在水中的沉淀溶解平衡曲线如图,可知Ag2SO4在此温度下的溶度积常数(Ksp)为8×10-4 |
8.取用液体药品时,正确的操作是( )
| A. | 手拿试剂瓶,标签向外 | |
| B. | 试剂瓶口不要紧贴试管口,以防污染 | |
| C. | 手持试管,应垂直拿 | |
| D. | 取完药品盖好瓶盖,放回原处,标签向外 |
5.下列有机物分子中有手性的是( )
| A. | 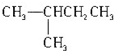 | B. | HCHO | ||
| C. | 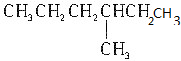 | D. | 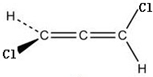 |
2.下列实验操作合理的是( )
| A. | 用酒精萃取碘水中的碘 | B. | 用托盘天平称取5.20 g氯化钠 | ||
| C. | 用100 mL量筒量取5.2mL盐酸 | D. | 用蒸馏可以除去水中的Fe3+等杂质 |
3.用NA表示阿伏加德罗常数,N表示微粒数,下列说法正确的是( )
| A. | 氯气与水发生反应,氯气在反应中减少1mol,溶液中生成的HClO分子数恰好为NA | |
| B. | 标准状况下,足量的Fe与2.24 L Cl2反应转移电子的数目为0.3NA | |
| C. | 100 mL pH=2的新制氯水中:N(OH-)+2N(ClO-)+N(HClO)=0.001 NA | |
| D. | 1.6 g CH4含有共用电子对的数目为0.5NA |