题目内容
设NA为阿伏伽德罗常数,下列有关叙述不正确的是( )
| A、常温常压下,1mol甲基(-CH30)所含的电子数为9NA |
| B、质子总数为5NA的重水(D2O)物质的量是0.5mol |
| C、0.1molK2O2与水反应时,转移的电子数为0.2NA |
| D、常温常压下,NA个甲烷分子的体积大于22.4L |
考点:阿伏加德罗常数
专题:
分析:A、依据甲基是中性取代基分析;
B、1mol重水含10mol质子;
C、过氧化钠中氧元素为-1价,1molNa2O2与水完全反应生成0.5mol氧气,转移了1mol电子;
D、常温常压下,气体摩尔体积大于22.4L/mol.
B、1mol重水含10mol质子;
C、过氧化钠中氧元素为-1价,1molNa2O2与水完全反应生成0.5mol氧气,转移了1mol电子;
D、常温常压下,气体摩尔体积大于22.4L/mol.
解答:
解:A、甲基是中性取代基,1mol甲基所含的电子数为9NA,故A正确;
B、1mol重水含10mol质子,故质子总数为5NA的重水(D2O)物质的量是0.5mol,故B正确;
C、1molNa2O2与水完全反应生成0.5mol氧气,转移了1mol电子,故0.1mol过氧化钠转移电子数为0.1NA,故C错误;
D、常温常压下,气体摩尔体积大于22.4L/mol,故常温常压下,NA个甲烷分子的体积大于22.4L,故D正确.
故选C.
B、1mol重水含10mol质子,故质子总数为5NA的重水(D2O)物质的量是0.5mol,故B正确;
C、1molNa2O2与水完全反应生成0.5mol氧气,转移了1mol电子,故0.1mol过氧化钠转移电子数为0.1NA,故C错误;
D、常温常压下,气体摩尔体积大于22.4L/mol,故常温常压下,NA个甲烷分子的体积大于22.4L,故D正确.
故选C.
点评:本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
相关题目
合成氨所需的氢气由煤与水发生反应制得,其中一步反应为:CO(g)+H2O(g)?CO2(g)+H2(g);△H<0,要使CO转化率提高,可采用下列措施中的( )
| A、增大水蒸气的浓度 |
| B、增大CO的浓度 |
| C、升高温度 |
| D、增大压强 |
设NA表示阿伏加德罗常数的值,下列叙述中正确的是( )
| A、16g O3与 O2混合物中所含氧原子数为NA |
| B、2.3gNa+中含有的电子数为0.1NA |
| C、在常温常压下11.2L二氧化碳所含的分子数目为0.5NA |
| D、相同质量的两块钠分别变成氧化钠和过氧化钠前者失去的电子数多 |
下列变化过程,属于放热反应的是( )
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
①水蒸气变成液态水
②酸碱中和反应
③浓H2SO4稀释
④固体NaOH溶于水
⑤H2在Cl2中燃烧
⑥弱酸的电离.
| A、②③④⑤ | B、②③④ |
| C、②⑤ | D、①②③④⑤ |
现有下列四种因素:①温度和压强 ②所含微粒数 ③微粒本身大小 ④微粒间的距离,其中对气体物质体积有显著影响的是( )
| A、只②③④ | B、只①②④ |
| C、只①③④ | D、①②③④全部 |
下列电子式正确的是( )
A、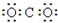 |
B、 |
C、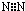 |
D、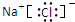 |
下列离子方程式书写正确的是( )
| A、铁与盐酸反应:Fe+2H+=Fe3++H2↑ |
| B、氢氧化钡溶液和稀硫酸反应:Ba2++SO42-=BaSO4↓ |
| C、氯化铝中加入过量的氨水:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| D、向水玻璃中加盐酸:SiO32-+2H+=H2SiO3↓ |