题目内容
某化学兴趣小组为研究过氧化钠与SO2的反应情况,进行如下探究.
(1)[提出假设]
向一定量的过氧化钠固体中通人足量的SO2,对反应后的固体产物成分及反应原理提出如下假设:
假设一:反应后固体中只有Na2SO3,证明SO2未被氧化;
假没二:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设三:反应后固体中 ,明SO2部分被氧化.
(2)[定性研究]
为验证假设三,该小组进行如下研究,请你完成下表中内容.
(3)[定量研究]
通过测量气体的体积判断发生的化学反应,实验装置如下:

①B中所盛装试剂的名称为 .
②装置D的作用是
③请画出实验装置E.
④实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g.装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据进行填表判断.
(1)[提出假设]
向一定量的过氧化钠固体中通人足量的SO2,对反应后的固体产物成分及反应原理提出如下假设:
假设一:反应后固体中只有Na2SO3,证明SO2未被氧化;
假没二:反应后固体中只有Na2SO4,证明SO2完全被氧化;
假设三:反应后固体中
(2)[定性研究]
为验证假设三,该小组进行如下研究,请你完成下表中内容.
| 实验步骤(不要求写出具体操作过程) | 预期的实验现象和结论 |
| 取适量反应后的固体放入试管中, |
通过测量气体的体积判断发生的化学反应,实验装置如下:

①B中所盛装试剂的名称为
②装置D的作用是
③请画出实验装置E.
④实验测得装置C中过氧化钠质量增加了m1g,装置D质量增加了m2g.装置E中收集到的气体为VL(已换算成标准状况下),用上述有关测量数据进行填表判断.
| SO2被氧化的程度 | V与m1或m2的关系 |
| 未被氧化 | |
| 完全被氧化 | V=0 |
| 部分被氧化 |
考点:二氧化硫的化学性质,探究物质的组成或测量物质的含量
专题:实验探究和数据处理题,氧族元素
分析:(1)依据假设一和假设二推断假设三为Na2SO3和Na2SO4的混合物;
(2)要证明假设3是否成立,应证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①从装置A中出来的气体含有水蒸汽,应用B装置除去水;
②二氧化硫为酸性氧化物,可以用碱石灰吸收;
③若Na2SO3未被氧化,则与过氧化钠反应生成氧气,氧气难溶于水,可以用排水法测量生成氧气的体积;
④若Na2SO3未被氧化发生的反应只有2Na2O2+2SO2=2Na2SO3+O2根据差量法计算;
(2)要证明假设3是否成立,应证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①从装置A中出来的气体含有水蒸汽,应用B装置除去水;
②二氧化硫为酸性氧化物,可以用碱石灰吸收;
③若Na2SO3未被氧化,则与过氧化钠反应生成氧气,氧气难溶于水,可以用排水法测量生成氧气的体积;
④若Na2SO3未被氧化发生的反应只有2Na2O2+2SO2=2Na2SO3+O2根据差量法计算;
解答:
解:(1)依据假设一和假设二推断假设三为Na2SO3和Na2SO4的混合物;
故答案为:Na2SO3和Na2SO4的混合物;
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠,
故答案为:加少量水溶解,加入氯化钡,再加热稀盐酸;
加入氯化钡溶于有白色沉淀,加热颜色沉淀部分溶解,证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①从装置A中出来的气体含有水蒸汽,二氧化硫为酸性气体,不能选择碱性干燥剂,浓硫酸具有吸水性,可以除去二氧化硫中水,
故选:浓硫酸;
②二氧化硫为酸性氧化物,可以用碱石灰吸收,故D的作用吸收未反应的SO2;
故答案为:吸收未反应的二氧化硫;
③若亚硫酸钠未被氧化,则与过氧化钠反应生成氧气,氧气难溶于水,可以用排水法测量生成氧气的体积,所以E装置为: ;
;
故答案为: ;
;
④若SO2未被氧化、则发生反应:2Na2O2+2SO2=2Na2SO3+O2
依据化学方程式和反应增重计算E中收集的氧气:
2Na2O2+2SO2=2Na2SO3+O2△m
1mol 96g
实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),若SO2未被氧化、则发生反应:2Na2O2+2SO2=2Na2SO3+O2
依据化学方程式和反应增重计算E中收集的氧气:
2Na2O2+2SO2=2Na2SO3+O2 反应增重
1mol 96g
m1
解得V=
若二氧化硫全部被氧化发生的反应为:Na2O2+SO2=Na2SO4;反应过程中 无氧气生成,V=0;
所以若0<V<
则二氧化硫部分被氧化;
故答案为:
.
故答案为:Na2SO3和Na2SO4的混合物;
(2)要证明假设3是否成立,就是要证明Na2SO3和Na2SO4存在,可以取反应后的固体放入试管中,加少量水溶解,加入BaCl2溶液,再加入稀盐酸,若加入BaCl2溶液有白色沉淀产生,加入盐酸沉淀部分溶解,则证明原固体中既有亚硫酸钠也有硫酸钠,
故答案为:加少量水溶解,加入氯化钡,再加热稀盐酸;
加入氯化钡溶于有白色沉淀,加热颜色沉淀部分溶解,证明原固体中既有亚硫酸钠也有硫酸钠;
(3)①从装置A中出来的气体含有水蒸汽,二氧化硫为酸性气体,不能选择碱性干燥剂,浓硫酸具有吸水性,可以除去二氧化硫中水,
故选:浓硫酸;
②二氧化硫为酸性氧化物,可以用碱石灰吸收,故D的作用吸收未反应的SO2;
故答案为:吸收未反应的二氧化硫;
③若亚硫酸钠未被氧化,则与过氧化钠反应生成氧气,氧气难溶于水,可以用排水法测量生成氧气的体积,所以E装置为:
 ;
;故答案为:
 ;
;④若SO2未被氧化、则发生反应:2Na2O2+2SO2=2Na2SO3+O2
依据化学方程式和反应增重计算E中收集的氧气:
2Na2O2+2SO2=2Na2SO3+O2△m
1mol 96g
实验测得装置C中过氧化钠质量增加了m1 g,装置D质量增加了m2 g,装置E中收集到的气体为V L(已换算成标准状况下),若SO2未被氧化、则发生反应:2Na2O2+2SO2=2Na2SO3+O2
依据化学方程式和反应增重计算E中收集的氧气:
2Na2O2+2SO2=2Na2SO3+O2 反应增重
1mol 96g
| V |
| 22.4L/mol |
解得V=
| 7m1 |
| 30 |
若二氧化硫全部被氧化发生的反应为:Na2O2+SO2=Na2SO4;反应过程中 无氧气生成,V=0;
所以若0<V<
| 7m1 |
| 30 |
故答案为:
| 7m1 |
| 30 |
点评:本题考查了二氧化硫性质应用和实验验证,实验设计的步骤和实验方案的确,明确物质的性质是解题关键,题目难度中等.

练习册系列答案
相关题目
美国科学家最近发明了利用眼泪来检测糖尿病的装置,其原理是利用氯金酸钠(NaAuCl4)溶液与眼泪中的葡萄糖反应生成纳米金单质颗粒(直径为20nm~60nm),下列说法中错误的是( )
| A、葡萄糖具有还原性 |
| B、葡萄糖的结构简式CH2OH(CHOH)4CHO |
| C、检测时NaAuCl4发生氧化反应 |
| D、纳米金单质颗粒分散在水中所得的分散系能产生丁达尔效应 |
香兰素是重要的香料之一,它可由丁香酚经多步反应合成,有关上述两种化合物的说法正确的是( )
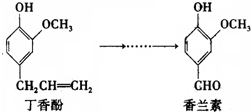

| A、香兰素分子中至少有12个原子共平面 |
| B、丁香酚不能与三氯化铁溶液发生显色反应 |
| C、1mol香兰素最多能与3mol氢气发生加成反应 |
| D、常温下1mol丁香酚只能与1molBr2反应 |
下列各组离子在溶液中能大量共存的是( )
| A、Na+、OH-、S2O32-、Cl- |
| B、Fe2+、K+、[Fe(CN)6]3-、NO3- |
| C、H+、C2O42-、MnO4-、SO42- |
| D、Na+、Ca2+、AlO2-、HCO3- |
下列不能通过化合反应得到的是( )
| A、氢氧化铁 | B、氢氧化铝 |
| C、盐酸 | D、碳酸氢钠 |
下列各项比较中前者高于(或大于或强于)后者的是( )
| A、CH4和SiH4的熔点 |
| B、I2在H2O中的溶解能力和I2在CCl4中的溶解能力 |
| C、H2SO3和H2SO4的酸性 |
D、对羟基苯甲醛( )和邻羟基苯甲醛( )和邻羟基苯甲醛( )的沸点 )的沸点 |
在向铝铵矾溶液中逐滴滴加氢氧化钡溶液的过程中,下列关系可能正确的是 ( )
| A、n(SO42-)>n(NH4+)>n(Al3+)>n(OH-) |
| B、n(Al3+)>n(NH4+)>n(SO42-)>n(H+) |
| C、n(BaSO4)>n[Al(OH)3]>n(NH3?H2O)>n(AlO2-) |
| D、n(NH3?H2O)>n(BaSO4)>n[Al(OH)3]>n(AlO2-) |