题目内容
16.亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组用下图所示装置制备NaNO2并对其性质作如下探究(A中加热装置已略去).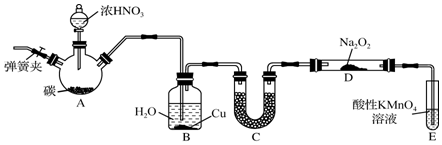
已知:①2NO+Na2O2═2NaNO2;
②NO能被酸性KMnO4氧化成NO3-,MnO4-被还原为Mn2+.
I.制备NaNO2
(1)装置A三颈烧瓶中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的目的是将NO2转化为NO;铜与稀硝酸反应生成NO.
(3)为保证制得的亚硝酸钠的纯度,C装置中盛放的试剂可能是BD(填序号).
A.P2O5 B.碱石灰 C.无水CaCl2 D.生石灰
(4)E装置发生反应的离子方程式是5NO+3MnO4-+4H+=5NO3-+3 Mn2++2H20.
II.测定NaNO2纯度
(5)准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解.用a mol•L-1酸性KMnO4溶液滴定,达滴定终点时所用KMnO4溶液体积为bml.则样品中NaNO2的质量分数为$\frac{69ab}{4m}%$.
(假设样品中其他杂质与酸性KMnO4溶液不反应,用含m、a、b的代数式表示.)
分析 Ⅰ.制备NaNO2并对其性质作探究,由实验装置可知,A中发生C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,B中稀释挥发的硝酸和生成的二氧化氮,C中固体干燥剂干燥NO,并除去可能混有的酸雾,D中发生2NO+Na2O2═2NaNO2,E中高锰酸钾吸收尾气NO,
(1)A中是碳和浓硝酸发生的反应生成二氧化碳、二氧化氮和水;
(2)B中稀释挥发的硝酸和生成的二氧化氮,使二氧化氮转化为NO,同时稀硝酸和铜发生反应;
(3)保证气体中酸性气体吸收,一氧化氮气体干燥;
(4)E装置的作用是吸收有毒的NO气体,避免污染空气;
II.测定NaNO2纯度
(5)将NaNO2滴加到酸性高锰酸钾溶液中,可观察到紫色溶液颜色变浅,直至褪色,说明二者发生氧化还原反应,亚硝酸根离子被氧化生成硝酸根离子,高锰酸根离子被还原生成锰离子,结合化学反应的定量关系计算;
解答 解:(1)装置A三颈烧瓶中发生反应的化学方程式为C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(2)B装置的目的是①将NO2转化为NO、②铜与稀硝酸反应生成NO,故答案为:将NO2转化为NO;铜与稀硝酸反应生成NO;
(3)A、C不能吸收酸,B、D可吸收酸且干燥气体,故答案为:BD;
(4)由信息可知,E装置的作用是利用高锰酸钾溶液的强氧化性氧化吸收有毒气体一氧化氮,吸收有毒的NO气体,避免污染空气,反应的离子方程式为:5NO+3MnO4-+4H+=5NO3-+3 Mn2++2H20,
故答案为:5NO+3MnO4-+4H+=5NO3-+3 Mn2++2H20;
(5)将NaNO2滴加到酸性高锰酸钾溶液中,可观察到紫色溶液颜色变浅,直至褪色,说明二者发生氧化还原反应,亚硝酸根离子被氧化生成硝酸根离子,高锰酸根离子被还原生成锰离子,将NaNO2滴加到酸性高锰酸钾溶液中,可观察到紫色溶液颜色变浅,直至褪色,说明二者发生氧化还原反应,亚硝酸根离子被氧化生成硝酸根离子,高锰酸根离子被还原生成锰离子,离子方程式为,准确称取质量为m g的NaNO2样品放入锥形瓶中,加适量水溶解.用a mol•L-1酸性KMnO4溶液滴定,达滴定终点时所用KMnO4溶液体积为bml.
2MnO4-+5NO2-+6H+=2Mn 2++3H2O+5NO3-,
2 5
amol/L×b×10-3L n
n=$\frac{5a×b×1{0}^{-3}}{2}$mol
则样品中NaNO2的质量分数为$\frac{\frac{5a×b×1{0}^{-3}}{2}mol×69g/mol}{mg}$×100%=$\frac{69ab}{4m}%$,
故答案为:$\frac{69ab}{4m}%$;
点评 本题考查物质的制备实验,为高频考点,把握制备实验原理、实验装置的作用、氧化还原反应的应用为解答的关键,侧重分析与实验及应用能力的综合考查,题目难度中等.

 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案 .
. 用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )
用如图表示的一些物质或概念之间的从属或包含关系中,错误的是( )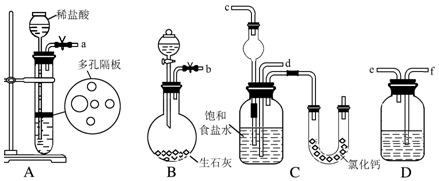
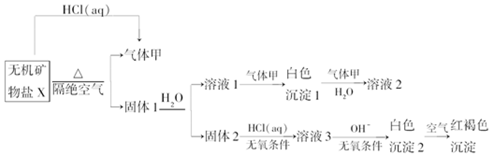
 ,写出气体甲的电子式
,写出气体甲的电子式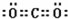 .
.
