题目内容
在密闭容器中的可逆反应CO(g)+NO2(g)?CO2(g)+NO(g)+Q(Q>0)达到平衡后:
(1)扩大容器体积,平衡 移动,C(NO2)将 ,反应混合物的颜色 .
(2)升高温度平衡 移动,体系的压强 .
(3)加入催化剂,NO的物质的量 .
(1)扩大容器体积,平衡
(2)升高温度平衡
(3)加入催化剂,NO的物质的量
考点:化学平衡的影响因素
专题:化学平衡专题
分析:(1)由于反应前后气体的化学计量数之和相等,压强对平衡移动没有影响,但反应物的浓度减小;
(2)反应是放热反应,升温平衡向逆反应方向移动;
(3)催化剂对平衡移动无影响.
(2)反应是放热反应,升温平衡向逆反应方向移动;
(3)催化剂对平衡移动无影响.
解答:
解:可逆反应CO(g)+NO2(g)?CO2(g)+NO(g)+Q(Q>0),该反应中,气体的化学计量数之和前后相等,反应放热,则:
(1)由于反应前后气体的化学计量数之和相等,压强对平衡移动没有影响,但由于体积增大,气体压强减小,气体的物质的量不变,所以反应物的浓度减小,反应混合物的颜色变浅,故答案为:不移动;减小;变浅;
(2)反应是放热反应,升高温度,平衡向逆反应方向移动,反应前后气体的化学计量数之和相等,混合气体分子数不变,故答案为:逆向;不变;
(3)催化剂只改变反应速率,但不改变平衡移动,所以加入催化剂对平衡移动无影响,故答案为:不变.
(1)由于反应前后气体的化学计量数之和相等,压强对平衡移动没有影响,但由于体积增大,气体压强减小,气体的物质的量不变,所以反应物的浓度减小,反应混合物的颜色变浅,故答案为:不移动;减小;变浅;
(2)反应是放热反应,升高温度,平衡向逆反应方向移动,反应前后气体的化学计量数之和相等,混合气体分子数不变,故答案为:逆向;不变;
(3)催化剂只改变反应速率,但不改变平衡移动,所以加入催化剂对平衡移动无影响,故答案为:不变.
点评:本题考查化学平衡的影响因素,题目难度不大,解答时首先分析化学方程式的特征,特别是反应前后气体的化学计量数关系以及反应的吸、放热问题.

练习册系列答案
相关题目
将含杂质的4.0克NaOH固体配成1000mL溶液取20mL置于锥形瓶中,用0.1mol/L盐酸滴定(甲基橙作指示剂),消耗盐酸19.6mL,则NaOH中含有杂质可能是( )
| A、Na2O |
| B、Na2CO3 |
| C、NaHCO3 |
| D、Ca(OH)2 |
下列说法正确的是( )
| A、化学反应的限度决定于反应物的性质,与外界条件无关 |
| B、合成氨反应在一定条件下达到平衡后,N2、H2、NH3物质的量之比保持恒定 |
| C、增大反应物的用量一定会加快反应速率 |
| D、浓度、温度、压强、催化剂既是影响反应速率的因素又是影响反应限度的因素 |
下列说法中,正确的是( )
| A、铜锌原电池中,电子由锌极经导线流向铜极 |
| B、铜锌原电池中,锌作阳极,铜作阴极 |
| C、石墨电极电解氯化铜溶液的反应中,阳极上质量增重 |
| D、石墨电极电解氯化钠溶液的反应中,用氢氧化钠溶液吸收阴极产物 |
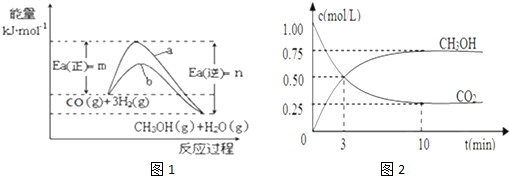
 氨气是生产氮肥、硝酸、纯碱等的重要原料.
氨气是生产氮肥、硝酸、纯碱等的重要原料.