题目内容
15.下列物质中不属于电解质的是( )| A. | KOH | B. | CuCl2 | C. | H2SO4 | D. | 蔗糖 |
分析 电解质是指:该物质是化合物,溶于水溶液中或在熔融状态下就能够导电,是自身电离.酸、碱、盐都是电解质,在水溶液中和在熔融状态下两种情况下都不能导电的化合物称为非电解质,蔗糖、乙醇等都是非电解质.大多数的有机物都是非电解质;单质,混合物既不是电解质也不是非电解质.
解答 解:A.KOH在水溶液里或在熔融状态下,能电离出自由移动的钠离子和氢氧根离子导致导电,所以KOH是电解质,故A不选;
B.CuCl2在水溶液里或在熔融状态下,能电离出自由移动的铜离子和氯离子导致导电,所以CuCl2是电解质,故B不选;
C.H2SO4在水溶液里,能电离出自由移动的氢离子和硫酸根离子导致导电,所以H2SO4是电解质,故C不选;
D.蔗糖是化合物,在水溶液里存在蔗糖分子,没有自由移动的离子,故不能导电,是非电解质,不属于电解质,故D选;
故选D.
点评 本题较简单,主要考查电解质的定义,注意电解质和非电解质都必须是化合物,电解质能导电是溶于水溶液中或在熔融状态下自身电离,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.葡萄酒中的酒精是葡萄果实中的糖发酵后的产物(C6H12O6$\stackrel{酵母}{→}$2CH3CH2OH+2CO2↑).
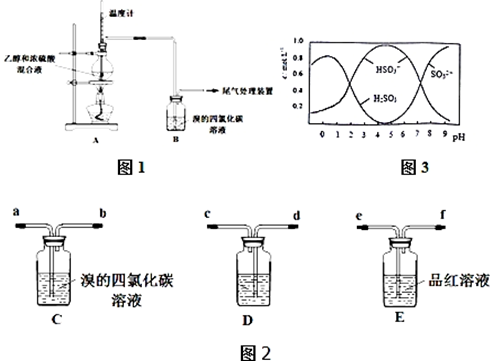
Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
(1)溶液“渐渐变黑”,说明浓硫酸具有脱水性.
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp=1×10-10,Ksp=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全,此时溶液中c(SO32-)≤0.05mol•L-1.

Ⅰ、已知:实验室制乙烯原理为CH3CH2OH$→_{170℃}^{浓硫酸}$CH2═CH2↑+H2O,产生的气体能使Br2 的四氯化碳溶液褪色,甲、乙同学用下列实验验证.(气密性已检验,部分夹持装置略如图1).
实验操作和现象:
| 操 作 | 现 象 |
| 点燃酒精灯,加热至170℃ | Ⅰ:A中烧瓶内液体渐渐变黑 Ⅱ:B内气泡连续冒出,溶液逐渐褪色 |
| … | |
| 实验完毕,清洗烧瓶 | Ⅲ:A中烧瓶内附着少量黑色颗粒状物,有刺激性气味逸出 |
(2)分析,甲认为是C2H4,乙认为不能排除SO2的作用.
①根据甲的观点,使B中溶液褪色反应的化学方程式是CH2=CH2+Br2→CH2Br-CH2Br;
②乙根据现象认为实验中产生的SO2和H2O,使B中有色物质反应褪色.
③为证实各自观点,甲、乙重新实验,设计与现象如下:
甲:在A、B间增加一个装有某种试剂的洗气瓶;现象:Br2的CCl4溶液褪色.
乙:用下列装置按一定顺序与A连接:(尾气处理装置略如图2)
现象:C中溶液由红棕色变为浅红棕色时,E中溶液褪色.
请回答下列问题:
a.甲设计实验中A、B间洗气瓶中盛放的试剂是NaOH溶液;乙设计的实验D中盛放的试剂是浓硫酸,装置连接顺序为(d)cabe(f).
b.能说明确实是SO2使E中溶液褪色的实验是加热已经褪色的品红溶液,若红色恢复,证明是SO2使品红溶液褪色而不是Br2.
c.乙为进一步验证其观点,取少量C中溶液,加入几滴BaCl2溶液,振荡,产生大量白色沉淀,浅红棕色消失,发生反应的离子方程式是SO2+2H2O+Br2═4H++2Br-+SO42-、SO42-+Ba2+═BaSO4↓或SO2+2H2O+Br2+Ba2+═4H++2Br-+BaSO4↓.
由此可得出的干燥的SO2 不能使Br2 的四氯化碳溶液褪色
Ⅱ、葡萄酒中常用Na2S2O5做抗氧化剂.
(3)0.5molNa2S2O5溶于水配成1L溶液,该溶液的pH=4.5.溶液中部分微粒浓度随溶液酸碱性变化如图3所示.写出Na2S2O5溶于水时发生的化学方程式Na2S2O5+H2O=2NaHSO3.
(4)已知:Ksp=1×10-10,Ksp=5×10-7.把部分被空气氧化的该溶液的pH调为10,向溶液中滴加BaCl2溶液使SO42-沉淀完全,此时溶液中c(SO32-)≤0.05mol•L-1.
6.我国晋代炼丹家、医学家葛洪所著《抱扑子》一书中记载有“丹砂烧之成水银,积变又还成丹砂”,其中丹砂是红色的硫化汞.下列说法正确的是( )
| A. | 汞可与稀硫酸反应生成氢气 | |
| B. | 丹砂在空气中灼烧发生了分解反应 | |
| C. | 水银在空气中继续加热又生成硫化汞 | |
| D. | 水银温度计打碎时,立即用纸槽收集洒落的汞珠即可 |
10.下列反应的离子方程式中,书写正确的是( )
| A. | 钠跟水反应:Na+2H2O═Na++2OH-+H2↑ | |
| B. | 向硫酸溶液中加入Ba(OH)2溶液:H++SO42-+Ba2++OH-═H2O+BaSO4↓ | |
| C. | 向A12(SO4)3溶液中加入过量的氨水:A13++3NH3•H2O═A1(OH)3↓+3NH4+ | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
7.下列离子方程式正确的是( )
| A. | 向烧碱溶液中通入少量二氧化碳:2OH-+CO2═CO32-+H2O | |
| B. | 向明矾溶液中滴加过量氨水:Al3++4OH-═AlO2-+2H2O | |
| C. | 向纯碱溶液中加入少量醋酸:CO32-+H+═HCO3- | |
| D. | 向小苏打溶液中加入少量石灰水:HCO3-+OH-═CO32-+H2O |
13.下列各组离子中,能在溶液中大量共存的一组是( )
| A. | Mg2+、Al3+、Cl-、OH- | B. | Na+、Ba2+、OH-、SO42- | ||
| C. | K+、Na+、NO3-、HCO3- | D. | K+、NH4+、CO32-、OH- |
14.已知反应4CO+2NO2?N2+4CO2在不同条件下的化学反应速率如下,其中表示反应速率最慢的是( )
| A. | v(CO)=1.5 mol•L-1•min-1 | B. | v(NO2)=0.7 mol•L-1•min-1 | ||
| C. | v(N2)=0.4 mol•L-1•min-1 | D. | v(CO2)=1.1 mol•L-1•min-1 |
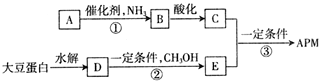
 .C中所含官能团的名称为羧基、氨基.
.C中所含官能团的名称为羧基、氨基. .
.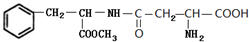 和
和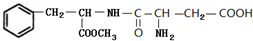 .
.