题目内容
下列反应的离子方程式书写正确的是( )
| A、石灰水中通入少量CO2:Ca2++2OH-+CO2=CaCO3↓+H2O |
| B、稀 H2SO4与铁粉反应:2Fe+6H+=2Fe3++3H2↑ |
| C、氢氧化钡溶液与稀 H2SO4 反应:Ba2++SO42-=BaSO4↓ |
| D、碳酸钙与盐酸反应:CO32-+2H+=H2O+CO2↑ |
考点:离子方程式的书写
专题:离子反应专题
分析:A、石灰水中通入少量CO2,生成碳酸钙;
B、稀硫酸是弱氧化剂,只能铁氧化为亚铁离子;
C、漏掉一组离子反应,而且相关离子要符合组成之比;
D、碳酸钙不溶于水,离子方程式中应写成化学式.
B、稀硫酸是弱氧化剂,只能铁氧化为亚铁离子;
C、漏掉一组离子反应,而且相关离子要符合组成之比;
D、碳酸钙不溶于水,离子方程式中应写成化学式.
解答:
解:A、石灰水中通入少量CO2,生成碳酸钙,正确的离子方程式为Ca2++2OH-+CO2=CaCO3↓+H2O,故A正确;
B、稀硫酸是弱氧化剂,只能铁氧化为亚铁离子,正确的离子方程式为Fe+2H+=Fe2++H2↑,故B错误;
C、漏掉一组离子反应,而且相关离子要符合组成之比,离子方程式为2H++2OH-+Ba2++SO42-=BaSO4↓+2H2O,故C错误;
D、碳酸钙不溶于水,离子方程式中应写成化学式,离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故D错误;
故选A.
B、稀硫酸是弱氧化剂,只能铁氧化为亚铁离子,正确的离子方程式为Fe+2H+=Fe2++H2↑,故B错误;
C、漏掉一组离子反应,而且相关离子要符合组成之比,离子方程式为2H++2OH-+Ba2++SO42-=BaSO4↓+2H2O,故C错误;
D、碳酸钙不溶于水,离子方程式中应写成化学式,离子方程式为CaCO3+2H+=Ca2++CO2↑+H2O,故D错误;
故选A.
点评:本题考查离子方程式的书写,题目难度不大,注意从化学式、离子符号、电荷守恒以及是否符合反应实际的角度分析.

练习册系列答案
相关题目
已知断裂1mol C-H键,要吸收热量414.4kJ;断裂1mol C-C键,要吸收热量347.4kJ;生成1mol C═C键,会放出热量615.3kJ;生成1mol H-H键,会放出热量435.3kJ,某有机物分解的反应可表示为: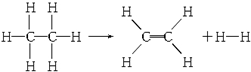
若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )

若在反应中消耗了1mol乙烷,则有关该反应的说法正确的是( )
| A、该反应放出251.2 kJ的热量 |
| B、该反应吸收251.2 kJ的热量 |
| C、该反应放出125.6 kJ的热量 |
| D、该反应吸收125.6 kJ的热量 |
由2-氯丙烷为主要原料制取1,2-丙二醇CH3CH(OH)CH2OH时,经过的反应为( )
| A、加成反应-消去反应-取代反应 |
| B、消去反应-加成反应-取代反应 |
| C、消去反应-取代反应-加成反应 |
| D、取代反应-加成反应-消去反应 |
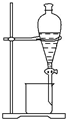
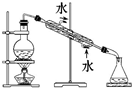
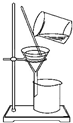
完成下列实验所需选择的装置或仪器都正确的是( )
| A | B | C | D | |
| 实验 | 分离植物油和氯化钠溶液 | 除去氯化钠晶体中混有的氯化钾晶体 | 分离CCl4中的Br2 | 除去CO2气体中的HCl气体 |
| 装置 或仪器 |
 |
 |
 |
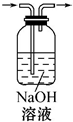 |
| A、A | B、B | C、C | D、D |
在密闭容器中于一定条件下进行下列反应:2SO2+O2?2SO3当到达平衡时通入18O2,再次平衡时,18O存在于( )
| A、SO2、O2 |
| B、SO2、SO3 |
| C、O2、SO3 |
| D、SO2、O2、SO3 |
下列说法中,正确的是( )
| A、强电解质的水溶液一定比弱电解质溶液的导电能力强 |
| B、强电解质都是离子化合物,弱电解质都是共价化合物 |
| C、强电解质的水溶液中不存在溶质分子 |
| D、不溶性盐都是弱电解质,可溶性酸和具有极性键的化合物都是强电解质 |
在恒温、恒容的密闭容器中进行反应A(g)?B(g)+C(g).若反应物的浓度由3mol?L-1降到1.8mol?L-1需30s,那么反应物浓度由0.8mol?L-1降至0.2mol?L-1所需反应时间为( )
| A、15 s |
| B、大于15 s |
| C、小于15 s |
| D、无法判断 |
下列关于元素周期律的叙述正确的是( )
| A、随着原子序数的递增,原子最外层电子数总是从1到8重复出现 |
| B、同主族元素的原子半径从上到下逐渐增大 |
| C、随着原子序数的递增,元素的最高正价从+1至+7,负价从-7至-1重复出现 |
| D、元素性质周期性变化是由原子半径周期性变化导致的 |
已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为( )
| A、1:3 | B、2:1 |
| C、1:1 | D、1:2 |