题目内容
请写出实验室制备CO2的化学方程式: 其离子方程式为: .
考点:离子方程式的书写
专题:离子反应专题
分析:实验室利用碳酸钙与盐酸反应制取二氧化碳,据此解题.
解答:
解:实验室利用碳酸钙与盐酸反应制取二氧化碳,该化学方程式:CaCO3+2HCl═CaCl2+CO2↑+H2O,离子反应为CaCO3+2H+═Ca2++CO2↑+H2O,
故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O;CaCO3+2H+═Ca2++CO2↑+H2O.
故答案为:CaCO3+2HCl═CaCl2+CO2↑+H2O;CaCO3+2H+═Ca2++CO2↑+H2O.
点评:本题考查离子反应的书写,明确发生的化学反应是解答本题的关键,题目难度中等.

练习册系列答案
相关题目
下列说法正确的是( )
| A、向AgCl悬浊液中加入少量NaCl固体后振荡,c(Cl-)增大,KsP (AgCl)增大 |
| B、某溶液中由水电离出的c(H+)=1.0×10-amol/L,若a>7时,则该溶液的pH一定为14-a |
| C、pH=3的二元弱酸H2R溶液与pH=11的NaOH溶液混合后溶液的pH等于7,则混合溶液中:c(R2-)+c(HR-)=c(Na+) |
| D、相同物质的量浓度的①NH4Al(SO4)2 ②NH4Cl③CH3COONH4 ④NH3?H2O溶液中,c(NH4+)由大到小的顺序是:①>②>③>④ |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A、在H2O2+Cl2═2HCl+O2反应中,每生成32 g氧气,则转移4 NA个电子 |
| B、常温下,4 g CH4含有NA个C-H共价键 |
| C、标准状态下,33.6 L氟化氢中含有1.5 N A个氟原子 |
| D、常温下,286 g Na2CO3?10H2O晶体中含有的CO32-小于NA个 |
设NA 表示阿伏加德罗常数的值.下列说法正确的是( )
| A、标准状况下,0.1 mol Cl2 溶于水,转移的电子数目为0.1NA |
| B、常温常压下,18 g H2O 中含有的原子总数为3NA |
| C、1 L 0.1 mol?L-1NaHCO3液含有0.1NA个HCO3- |
| D、常温常压下,2.24 L CO 和CO2 混合气体中含有的碳原子数目为0.1NA |
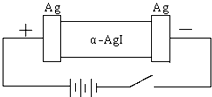 某同学查资料得知α-AgI是一种固体导体,导电率很高.他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如图所示(用铅蓄电池做电源)的电化学实验.已知铅蓄电池总反应:Pb+PbO2+2H2SO4
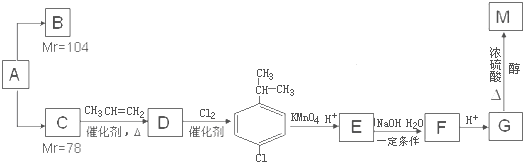
某同学查资料得知α-AgI是一种固体导体,导电率很高.他为了研究α-AgI究竟是Ag+离子导电还是I-离子导电,设计一个如图所示(用铅蓄电池做电源)的电化学实验.已知铅蓄电池总反应:Pb+PbO2+2H2SO4 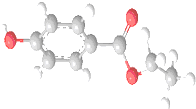 某相对分子质量为26的烃A,是一种重要的有机化工原料,以A为原料在不同的反应条件下可以转化为烃B、烃C,且B、C的核磁共振谱显示都只有一种氢.以C为原料通过下列方案可以制备具有广谱高效食品防腐作用的有机物M,M分子的球棍模型如图所示.
某相对分子质量为26的烃A,是一种重要的有机化工原料,以A为原料在不同的反应条件下可以转化为烃B、烃C,且B、C的核磁共振谱显示都只有一种氢.以C为原料通过下列方案可以制备具有广谱高效食品防腐作用的有机物M,M分子的球棍模型如图所示.