题目内容
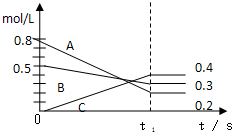 一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.依图中数据回答.
一定条件下气体A与气体B反应生成气体C,反应过程中反应物与生成物的浓度随时间变化的曲线如图.依图中数据回答.①该反应的化学方程式为
②反应从开始进行至时间t1,用气体B浓度变化表示的该反应的反应速率是
③此反应在达到平衡时,A的转化率为
考点:物质的量或浓度随时间的变化曲线
专题:化学平衡专题
分析:(1)根据图象中A、B、C浓度的变化趋势判断反应物和生成物,根据浓度变化之比等于化学剂量数之比确定反应的化学方程式;
(2)根据v=
计算反应速率;
(3)根据转化了的浓度与起始浓度之比可求得A的转化率;
(2)根据v=
| △c |
| △t |
(3)根据转化了的浓度与起始浓度之比可求得A的转化率;
解答:
解:(1)由图象可知,在反应中,A的浓度逐渐减小,B、C的浓度逐渐增大,则A、B为反应物,C为生成物,相同时间内浓度的变化比值为c(A):c(B):c(C)=(0.8-0.2):(0.5-0.3):0.4=3:1:2,化学反应中浓度变化之比等于化学剂量数之比,则化学方程式为3A+B 2C,故答案为:3A+B
2C,故答案为:3A+B 2C;
2C;
(2)反应从开始进行至时间t1,用气体B浓度变化表示的该反应的反应速率为:v=
=
=
mol?L-1?min-1,故答案为:
mol?L-1?min-1;
(3)根据转化了的浓度与起始浓度之比可求得A的转化率为
×100%=75%,故答案为:75%.
 2C,故答案为:3A+B
2C,故答案为:3A+B 2C;
2C;(2)反应从开始进行至时间t1,用气体B浓度变化表示的该反应的反应速率为:v=
| △c |
| △t |
| 0.5mol/L-0.3mol/L |
| t1 |
| o.2 |
| t1 |
| o.2 |
| t1 |
(3)根据转化了的浓度与起始浓度之比可求得A的转化率为
| 0.8mol/L-0.2mol/L |
| 0.8mol/L |
点评:本题考查了根据图象写方程式、化学反应速率的计算及转化率的计算,难度较小,解题关键是准确分析图表.

练习册系列答案
相关题目
下列气体的实验室制法正确的是( )
| A、O2:加热高锰酸钾固体 |
| B、CO2:大理石和稀硫酸反应 |
| C、NO:氮气和氧气反应 |
| D、NH3:加热氯化铵固体 |
下列各组元素性质递变情况错误的是( )
| A、P、S、Cl元素最高正化合价依次升高 |
| B、碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |
| C、S2-、Cl-、K+、Ca2+离子半径依次增大 |
| D、热稳定性:H2S>PH3>AsH3 |
下列说法或表示法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石)△H=+119kJ?mol-1可知,石墨比金刚石稳定 |
| C、在稀溶液中:H++OH-═H2O△H=-57.3kJ?mol-1,若将含1molCH3COOH的醋酸溶液与含1molNaOH的溶液混合,放出的热量等于57.3kJ |
| D、在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ?mol-1 |
下列离子方程式正确的是( )
| A、铜与硝酸银溶液反应:Cu+Ag+=Cu2++Ag |
| B、硫酸与氢氧化钡溶液反应:OH-+Ba2++SO42-+H+=BaSO4↓+H2O |
| C、碳酸钙和盐酸反应:CO32-+2H+=CO2↑+H2O |
| D、硫酸铜与氢氧化钡溶液反应:Cu2++SO42-+Ba2++2OH-=BaSO4↓+Cu(OH)2↓ |
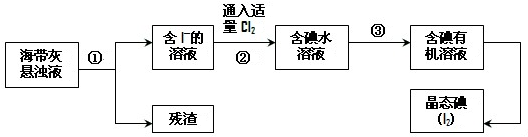
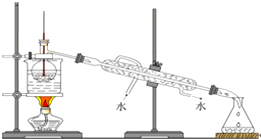
 Ⅰ.今运动场馆大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED晶片,材质基本以GaAs(砷化镓)、InGaN(氮化铟镓)为主.砷化镓作为第三代半导体,以其为材料制造的灯泡寿命长.耗能少.
Ⅰ.今运动场馆大量的照明材料或屏幕都使用了发光二极管(LED).目前市售LED晶片,材质基本以GaAs(砷化镓)、InGaN(氮化铟镓)为主.砷化镓作为第三代半导体,以其为材料制造的灯泡寿命长.耗能少.