题目内容
19.在一定温度下难溶盐AgCl的饱和溶液中,Ag+与Cl-的物质的量浓度类似于水中c(H+)和c(OH-)的关系,即c(Ag+)•c(Cl-)=Ksp(常数).在下列溶液中:①50mL 0.02mol/L AlCl3溶液,②30mL 0.02mol/L CaCl2溶液,③40mL 0.03mol/L盐酸,④10mL H2O,则AgCl的溶解度由大到小的顺序为( )| A. | ①②③④ | B. | ①④③② | C. | ④①②③ | D. | ④③②① |
分析 由c(Ag+)•c(Cl-)=Ksp可知,含Ag+或Cl-的溶解抑制AgCl的溶解,且离子浓度越大,AgCl的溶解度越小,以此来解答.
解答 解:①50mL 0.02mol/L AlCl3溶液中c(Cl-)=0.06mol/L;
②30mL 0.02mol/L CaCl2溶液中c(Cl-)=0.04mol/L;
③40mL 0.03mol/L盐酸中c(Cl-)=0.03mol/L;
④10mL H2O中c(Cl-)=c(Ag+)=0,
c(Ag+)或c(Cl-)浓度越大,AgCl的溶解度越小,
则AgCl的溶解度由大到小的顺序为④③②①,
故选D.
点评 本题考查溶度积的计算,为高频考点,把握溶解度与离子浓度的关系为解答的关键,侧重分析与计算能力的考查,注意溶解平衡的抑制作用,题目难度不大.

练习册系列答案
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案
相关题目
4.胶体分散系与其它分散系的本质差别是( )
| A. | 分散质直径大小 | B. | 分散质粒子是否带电 | ||
| C. | 是否稳定 | D. | 是否有丁达尔现象 |
14.一定温度下,存在溶解平衡关系:BaSO4(固体)?Ba2++SO42-.向该悬浊液中加入饱和Na2CO3溶液,下列叙述正确的是( )
已知Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=8.1×10-9.
已知Ksp(BaSO4)=1.1×10-10 Ksp(BaCO3)=8.1×10-9.
| A. | BaSO4一定能转化为BaCO3 | B. | BaSO4一定不能转化为BaCO3 | ||
| C. | BaSO4有可能转化为BaCO3 | D. | 无法通过实验来验证是否发生转化 |
11.若 A+酸=盐+水,则A不可能属于( )
| A. | 氧化物 | B. | 胶体 | C. | 碱 | D. | 单质 |
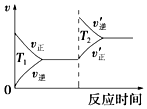
8.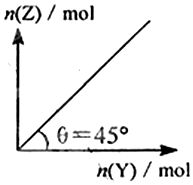 在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
 在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )
在一定温度和压强下,向盛有足量X的体积可变的密闭容器中通人Y气体,发生反应:X(s)+aY(g)?bZ(s)+W(g);△H>0平衡时Z的物质的量与通人Y的物质的量的变化关系如图所示.下列说法中正确的是( )| A. | 平衡时Y的转化率为$\frac{a}{b}$% | |
| B. | 向容器中再加入少量X,则Y的转化率增大 | |
| C. | 再通入Y,重新达到平衡时W的体积分数不变 | |
| D. | 保持压强一定,当原反应在较高温度下建立平衡时,图中θ<45° |
9.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况,1molH2O含O原子个数为NA | |
| B. | 1.12L N2中含N2分子数为0.05NA | |
| C. | 5.6gFe与足量稀盐酸反应,转移的电子数为0.3NA | |
| D. | 0.1molFeCl3可制得Fe(OH)3胶体的数目为0.1NA |
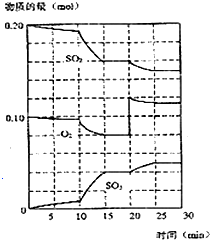 在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1
在450℃并有催化剂存在下,于一容积恒定的密闭容器内进行下列反应:2SO2(g)+O2(g)═2SO3(g)△H=-190kJ•mol-1