题目内容
5.下列物质晶体中,同时存在非极性键、极性键和氢键的是( )| A. | CaC2 | B. | H2O | C. | C2H4 | D. | H2O2 |
分析 同种非元素之间形成非极性共价键,不同非元素之间形成极性共价键,含有N、O、F的氢化物能形成氢键.
解答 解:A、CaC2中存在离子键和非极性共价键,无极性键和氢键,故A错误;
B、冰中存在极性键和氢键,无非极性键,故B错误;
C、C2H4晶体中存在极性键、非极性键,无氢键,故C错误;
D、H2O2晶体中存在极性键,非极性键和氢键,符合题意,故D正确;
故选D.
点评 本题主要考查了晶体中存在的化学键,掌握分子的结构是解题的关键,难度中等.

练习册系列答案
相关题目
15.化学在生产和日常生活中有着重要的应用.下列说法正确的是( )
| A. | 用米汤检验含碘盐中的碘元素 | |
| B. | 烧碱、小苏打、氢氧化铝均可用于治疗胃酸过多 | |
| C. | 工业生产中,常将氯气通入澄清石灰水中,制取漂白粉 | |
| D. | 除去CuSO4溶液中的Fe2(SO4)3,加入足量CuO粉末,充分搅拌过滤 |
16.“纳米材料”是粒子直径为几纳米至几十纳米的材料,纳米碳就是其中一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质 ①是溶液 ②是胶体 ③能产生丁达尔效应 ④不能透过滤纸 ⑤能透过滤纸 ⑥静置后会析出黑色沉淀( )
| A. | ①④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①③④⑥ |
17.下列实验操作能达到实验目的是( )
| 实验目的 | 实验内容 | |
| A | 配制氯化铁溶液 | 将氯化铁溶解在较浓的盐酸中,再加水稀释 |
| B | 探究温度对硫代硫酸钠与硫酸反应速率的影响 | 先将两种溶液混合并计时,再用水浴加热至设定温度 |
| C | 证明Ksp(BaSO4)<Ksp(CaSO4) | 室温下,向浓度均为0.1mol•L-1的BaCl2和CaCl2混合溶液中滴加Na2SO4溶液,出现白色沉淀. |
| D | HSO3-结合H+的能力比SO32-强 | 室温下,用pH试纸测得:0.1mol•L-1 Na2SO3溶液的pH约为10;0.1mol•L-1 NaHSO3溶液的pH约为5. |
| A. | A | B. | B | C. | C | D. | D |
7.设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,0.1 mol Cl2溶于水,转移的电子数目为0.1NA | |
| B. | 78 g Na2O2固体中含有的阴离子数为NA | |
| C. | 标准状况下,11.2 L CH3OH中含有的分子数目为0.5NA | |
| D. | 常温常压下,2.24 L CO和CO2混合气体中含有的碳原子数目为0.1NA |
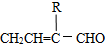 ,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
,水杨酸酯E为紫外吸收剂,可用于配制防晒霜.E的一种合成路线如下:
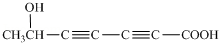 ;
;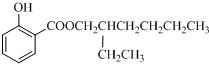 :
: .
.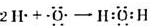 .
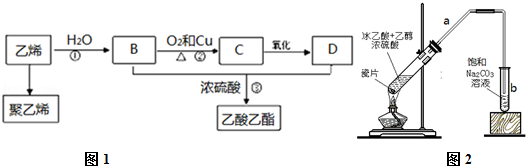
.
 ;
;