题目内容
10.元素的电负性用来描述不同元素的原子对键合电子吸引力的大小.电负性应用:判断元素的金属性和非金属性的强弱.下表列出了同周期的几种短周期元素的部分性质请回答下列问题:
| 元素符号 | A | B | C | D | E |
| 电负性 | 3.0 | 2.5 | X | 1.5 | 0.9 |
| 原子半径(单位nm) | 0.099 | 0.102 | 0.110 | 0.143 | 0.186 |
| 主要化合价 | -1,+7 | -2,+6 | -3,+5 | +3 | +1 |
 ;
;(2)X的值应为D(填字母);
A.3.6 B.3.1 C.1.4 D.2.1
(3)分析表中数据,简述同周期元素(除惰性气体)电负性大小与原子半径的关系:同周期元素的原子半径越小,电负性越大;
(4)A、B、C三种元素形成的氢化物中,其稳定性由强到弱的顺序是:HCl>H2S>PH3(用化学式表示)
(5)A、D最高价氧化物对应水化物相互反应的化学方程式:Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
分析 同周期短周期元素中,A有+7、-1价,为ⅦA族元素,A是Cl元素;B有-2、+6价,处于VIA族,B为S元素;C有-3、+5价,处于VA族,故C为P元素;D只有+3价,为ⅢA族元素,所以D是Al元素;E最高正价为+1,处于IA族,故E为Na,
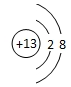
(1)铝离子核外电子数为10,有2个电子层,各层电子数为2、8;
(2)同周期自左而右电负性增大;
(3)同周期元素的原子半径越小,电负性越大;
(4)元素非金属性越强,氢化物越稳定;
(5)A、D最高价氧化物对应水化物分别为HClO4、Al(OH)3,二者反应生成Al(ClO4)3与水.
解答 解:由以上分析可知A为Cl、B为S、C为P、D为Al、E为Na元素.
(1)D是Al元素,对应的离子核外有2个电子层,最外层电子数为8,则Al3+ 结构示意图为 ,故答案为:
,故答案为: ;
;
(2)同周期自左而右电负性增大,P的电负性介于Al与硫之间,即介于1.5~2.5之间,故选:D;
(3)同周期元素的原子半径越小,电负性越大,故答案为:同周期元素的原子半径越小,电负性越大;
(4)非金属性Cl>S>P,元素非金属性越强,氢化物越稳定,故氢化物稳定性:HCl>H2S>PH3,故答案为:HCl>H2S>PH3;
(5)A、D最高价氧化物对应水化物分别为HClO4、Al(OH)3,二者反应生成Al(ClO4)3与水,反应方程式为:Al(OH)3+3HClO4═Al(ClO4)3+3H2O,故答案为:Al(OH)3+3HClO4═Al(ClO4)3+3H2O.
点评 本题考查位置结构性质关系应用,为高频考点,侧重考查学生的分析能力,关键是根据化合价及原子半径推断元素,注意对元素周期律的理解掌握,难度不大.

练习册系列答案
相关题目
20.茶叶中含有多种有益于人体健康的有机成分及钙、铁等微量金属元素,某化学研究性学习小组设计方案用以检验某品牌茶叶中铁元素的存在并测定钙元素的质量分数 (已知CaC2O4为白色沉淀物质).首先取200g茶叶样品进行如图1操作:请回答下列有关问题: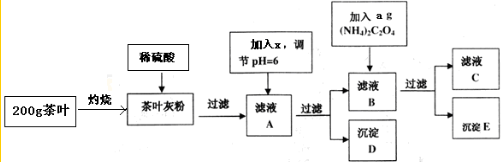
(1)①文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
②(NH4)3C2O4溶液显酸性
实验前要先将茶叶样品高温灼烧程灰粉,这部操作需要用到的实验仪器有:酒精灯、三脚架、玻璃棒、BC、其主要目的是使样品中的有机物完全分解.
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)从滤液A→沉淀D的过程中需要加入的物质X可以选择C
A.CaO B.Ca(OH)2 C.NH3•H2O
(3)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
现将滤液C稀释至250mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.10mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液体积如下表所示:
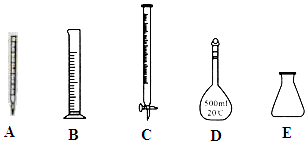
①此步操作过程中需要用到下列哪些仪器(如图)CDE(填写序号);
②滴定达到终点时的现象是滴入最后一滴KMnO4,溶液由无色变为紫色,且半分钟不恢复原色.
③为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,若不洗涤沉淀洗涤沉淀D,会使测定钙元素的含量偏低.(填“偏低”“偏高”、“无影响”,下同)若不洗涤沉淀E,会使测定钙元素的含量偏高.
④原茶叶中钙元素的质量分数为$\frac{\frac{a}{124}-0.05}{5}$.(用含a的代数式表示)
(4)设计最简单的实验检验茶叶中含有铁元素的操作和现象是:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素.

(1)①文献资料显示,某些金属离子的氢氧化物完全沉淀的pH为:
| 离子 | Ca2+ | Fe3+ |
| 完全沉淀时的pH | 13 | 4.1 |
实验前要先将茶叶样品高温灼烧程灰粉,这部操作需要用到的实验仪器有:酒精灯、三脚架、玻璃棒、BC、其主要目的是使样品中的有机物完全分解.
A.蒸发皿 B.坩埚 C.泥三角 D.石棉网
(2)从滤液A→沉淀D的过程中需要加入的物质X可以选择C
A.CaO B.Ca(OH)2 C.NH3•H2O
(3)用KMnO4标准溶液滴定C溶液时所发生的反应为:5C2O42-+2MnO4-+16H+=10CO2↑+2Mn2++8H2O
现将滤液C稀释至250mL,再取其中的25.00mL溶液,用硫酸酸化后,用0.10mol•L-1的KMnO4标准溶液滴定,终点时消耗KMnO4溶液体积如下表所示:
| 编号 | 终点时消耗KMnO4溶液体积(mL) |
| 1 | 19.98 |
| 2 | 22.00 |
| 3 | 20.02 |

②滴定达到终点时的现象是滴入最后一滴KMnO4,溶液由无色变为紫色,且半分钟不恢复原色.
③为保证实验精确度,沉淀D及E需要分别洗涤,并将洗涤液转移回母液中,若不洗涤沉淀洗涤沉淀D,会使测定钙元素的含量偏低.(填“偏低”“偏高”、“无影响”,下同)若不洗涤沉淀E,会使测定钙元素的含量偏高.
④原茶叶中钙元素的质量分数为$\frac{\frac{a}{124}-0.05}{5}$.(用含a的代数式表示)
(4)设计最简单的实验检验茶叶中含有铁元素的操作和现象是:取少量的滤液A,滴入硫氰化钾溶液,溶液变成红色,证明溶液中存在铁离子,也证明离子茶叶中含有铁元素.
18.下列设计的实验方案能达到实验目的是( )
| A. | 室温下,浓度均为0.1 mol•L-1Na2S2O3和H2SO4溶液,各取5 mL、10 mL的Na2S2O3溶液分别与10 mL的H2SO4溶液混合反应,验证Na2S2O3浓度对反应速率的影响 | |
| B. | 通过测定室温下等浓度的HNO3和H2SO4溶液的pH值,比较元素N、S的非金属性强弱 | |
| C. | KI--I2溶液中存在如下平衡:I2+I-?I3-.取V1mI平衡混合溶液,滴加几滴淀粉,用c mol/L的Na2S2O3溶液进行滴定(反应为I2+2Na2S2O3=2NaI+Na2S4O6),滴定终点时消耗V2 mL的Na2S2O3溶液.根据V1、V2和c可测定上述平衡体系中c(I2) | |
| D. | 确定铝片中氧化铝的含量:取一定质量的铝片,与过量的NaOH溶液充分反应,溢出的气体通过硅胶后,冷却至室温后准确测量其体积 |
15.下列可用于鉴别以下两种化合物的试剂是( )
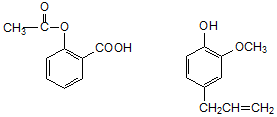

| A. | 银氨溶液 | B. | 稀溴水 | C. | 氯化铁溶液 | D. | 氢氧化钠溶液 |
2.用NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 电解精炼铜,当外电路通过NA个电子时;阳极质量减少32 g | |
| B. | 反应3H2(g)+N2(g)?2NH3(g)△H=-92kJ•mol-1,当放出热量 9.2 kJ时,转移电子0.6 NA | |
| C. | lmol•L1的氯化铜溶液中,若Cl-的数目为2Na,则Cu2+的数目为NA | |
| D. | 标准状况下,NO和O2各11.2L混合充分反应,所得气体的分子总数为0.75 NA |
19.工业上常用NaHSO3处理含Cr2O72-的废液,反应的离子方程式为:5H++Cr2O72-+3HSO3-→2Cr3++3SO42-+4H2O
下列判断错误的是( )
下列判断错误的是( )
| A. | 氧化产物是SO42- | |
| B. | 氧化剂与还原剂的物质的量之比是1:3 | |
| C. | Cr2O72-表现了氧化性 | |
| D. | 还原1molCr2O72-,电子转移3mol |
10.五种固体物质 A、B、C、D、E 由下表中不同的阴阳离子组成,它们均易溶于水.
分别取它们的水溶液进行实验,结果如下:
①A 溶液与 C 溶液混合后产生蓝色沉淀,向该沉淀中加入足量稀 HNO3,沉淀部分溶解,剩余 白色固体;
②B 溶液与 E 溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量 C 溶液与 D 溶液混合后产生白色沉淀,过量 C 溶液与 D 溶液混合后无现象;
④B 溶液与 D 溶液混合后无现象;
⑤将 38.4g Cu 片投入装有足量 D 溶液的试管中,Cu 片不溶解,再滴加 1.6mol/L 稀 H2SO4,Cu 逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断 A 的化学式为:ACuSO4;BFeCl3
(2)写出过量 C 与 D 发生反应的离子方程式Al3++4OH-=AlO2-+2H2O.
(3)B 溶液中滴入石蕊试液,现象是溶液变红,原因是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式说明)
分别取它们的水溶液进行实验,结果如下:
| 阳离子 | Na+ | Al3+ | Fe3+ | Cu2+ | Ba2+ |
| 阴离子 | OH- | Cl- | CO32- | NO3- | SO42- |
②B 溶液与 E 溶液混合后产生红褐色沉淀,同时产生大量气体;
③少量 C 溶液与 D 溶液混合后产生白色沉淀,过量 C 溶液与 D 溶液混合后无现象;
④B 溶液与 D 溶液混合后无现象;
⑤将 38.4g Cu 片投入装有足量 D 溶液的试管中,Cu 片不溶解,再滴加 1.6mol/L 稀 H2SO4,Cu 逐渐溶解,管口附近有红棕色气体出现.
(1)据此推断 A 的化学式为:ACuSO4;BFeCl3
(2)写出过量 C 与 D 发生反应的离子方程式Al3++4OH-=AlO2-+2H2O.
(3)B 溶液中滴入石蕊试液,现象是溶液变红,原因是Fe3++3H2O?Fe(OH)3+3H+(用离子方程式说明)