题目内容
下列化学反应的离子方程式书写正确的是( )
| A、将少量金属钠放人冷水中:Na+2H2O═Na++2OH-+H2↑ |
| B、将铝片加入烧碱溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ |
| C、向亚硫酸钠溶液中加入足量硝酸:SO32-+2H+═SO2↑+H2O |
| D、向澄清石灰水中通入过量二氧化碳:CO2+Ca2++2OH-═CaCO3↓+H2O |
考点:离子方程式的书写
专题:离子反应专题
分析:A.电子、电荷不守恒;
B.反应生成偏铝酸钠和氢气,电子、电荷守恒;
C.发生氧化还原反应生成硫酸根离子、NO和水;
D.反应生成碳酸氢钙.
B.反应生成偏铝酸钠和氢气,电子、电荷守恒;
C.发生氧化还原反应生成硫酸根离子、NO和水;
D.反应生成碳酸氢钙.
解答:
解:A.将少量金属钠放人冷水中的离子反应为2Na+2H2O═2Na++2OH-+H2↑,故A错误;
B.将铝片加入烧碱溶液中的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,故B正确;
C.向亚硫酸钠溶液中加入足量硝酸的离子反应为2NO3-+3SO32-+2H+═3SO42-+2NO↑+H2O,故C错误;
D.澄清石灰水中通入过量二氧化碳的离子反应为CO2+OH-═HCO3-,故D错误;
故选B.
B.将铝片加入烧碱溶液中的离子反应为2Al+2OH-+2H2O═2AlO2-+3H2↑,故B正确;
C.向亚硫酸钠溶液中加入足量硝酸的离子反应为2NO3-+3SO32-+2H+═3SO42-+2NO↑+H2O,故C错误;
D.澄清石灰水中通入过量二氧化碳的离子反应为CO2+OH-═HCO3-,故D错误;
故选B.
点评:本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、氧化还原反应的考查,注意电子、电荷守恒的应用,题目难度不大.

练习册系列答案
相关题目
下列关于命名的说法中错误的是( )
| A、所有烃类的命名都应选择含碳原子最多的链作主链,即“最多”原则 |
| B、二甲苯可以以邻、间、对这种习惯方法进行命名 |
| C、二甲苯也可以用系统方法进行命名 |
| D、化学式是C8H10的苯的同系物有4种同分异构体 |
下列说法中,可以证明反应N2+3H2?2NH3已达到平衡状态的是( )
①1个N≡N键断裂的同时有3个H-H键形成
②N2、H2、NH3的分子数之比为1:3:2
③1个N≡N键断裂的同时有6个N-H键形成
④N2、H2、NH3的浓度不再变化.
①1个N≡N键断裂的同时有3个H-H键形成
②N2、H2、NH3的分子数之比为1:3:2
③1个N≡N键断裂的同时有6个N-H键形成
④N2、H2、NH3的浓度不再变化.
| A、①④ | B、②③ | C、①③ | D、②④ |
下列有机物的命名正确的是( )
| A、Br-CH2-CH2-Br二溴乙烷: |
B、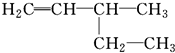 3-乙基-1-丁烯: 3-乙基-1-丁烯: |
C、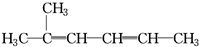 2-甲基-2,4-己二烯: 2-甲基-2,4-己二烯: |
D、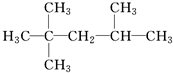 2,2,3-三甲基戊烷: 2,2,3-三甲基戊烷: |
氨能跟氧气在铂催化下反应生成硝酸和水,其中第一步反应为:4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(H2O)[mol?L-1?min-1]表示,则正确的关系是( )
| A、4v(NH3)=5v(O2) |
| B、5v(O2)=6v(H2O) |
| C、2v(NH3)=3v(H2O) |
| D、4v(O2)=5v(NO) |
下列说法中,不正确的是( )
| A、相对分子质量相同,组成元素的百分含量相同的不同有机物一定是同分异构体的关系 |
| B、碳原子数相同、结构不同的烷烃一定是互为同分异构体关系 |
| C、两有机物互为同系物,则它们也是互为同分异构体关系 |
| D、碳原子数≤10的烷烃,其一氯代物没有同分异构体的烷烃有4种 |
氨氧化制硝酸,吸收塔内发生反应 3NO2(g)+H2O(l)?2HNO3(aq)+NO△H<0 要提高反应的转化率,增加浓硝酸的产量,应采取的措施( )
| A、加压 | B、加大水量 |
| C、升温 | D、减压 |
下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
A、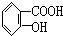 |
B、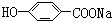 |
| C、H2NCH2COONa |
| D、Na2CO3 |
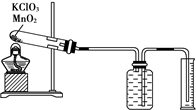 某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.实验步骤如下:
某同学设计了测定气体摩尔体积的探究实验,利用氯酸钾分解制O2.实验步骤如下: